Therapien mit umstrittener Wirksamkeit
In diesem Kapitel werden Therapien diskutiert, deren Wirksamkeit nicht vollends nachgewiesen werden konnte oder deren Wirksamkeit unklar ist. Dies ist besonders bei alternativen Behandlungsmöglichkeiten wie z.B. der Nahrungsmittelergänzung oder Stressmanagement der Fall. Ebenfalls sind Therapien aufgeführt, wie z.B. die medikamentöse Therapie mit Immunglobulinen, die keine Zulassung in Deutschland haben. Dieses Kapitel ist momentan noch im Aufbau.
Immunglobuline (z.B. Octagam®, Gamunex®, KIOVIG, Privigen®)
Dosierung und Anwendung
200mg/kg Körpergewicht monatlich (ca. 14 g) oder
400mg/kg Körpergewicht alle zwei Monate,
jeweils als Infusion über die Vene an einem Tag.
Qualität der Studien
⇑
Wirkung
Patienten ohne Zunahme einer Beeinträchtigung:

Krankheitsaktivitätsfreie Patienten
Jährliche Schubrate (Therapie/Plazebo)
0,52/1,26[1]
0,59/1,61[2]
Kernspin
KM-Herde:
T2-Herde:
Wirkmechanismus
Immunglobuline (IG) sind Antikörper, die im menschlichen Körper in vier Gruppen (A, G, M und E) vorkommen. Beim gesunden Menschen besteht ihre Hauptaufgabe in der Abwehr von Viren und Bakterien. Immunglobuline können bisher nur aus Blutspenden gewonnen werden. Durch Filtern von Blut können diese Antikörper gesammelt werden.
Aus dem Filtrat wird im nächsten Schritt ein flüssiges Medikament mit einer hohen Antikörperkonzentration hergestellt. Dazu müssen die Antikörper gereinigt und die Untergruppen herausgefiltert werden. Die therapeutisch eingesetzten IG stammen überwiegend aus der Klasse G.
Die IG werden über die Vene verabreicht. Darum wird die Therapie auch IVIG abgekürzt.
Die unterschiedlichen Wirkungsmechanismen von Immunglobulinen in der Therapie verschiedener entzündlicher Erkrankungen werden bisher noch nicht verstanden. Jedoch werden verschiedene Erklärungsansätze diskutiert:
- Zum einen können Eiweiße auf der Oberfläche von Blutzellen blockiert werden und eine Anlagerung von anderen Substanzen oder Zellen verhindert werden
- oder die Anlagerung führt direkt zu einer Veränderung der Zellreaktionen.
- Ferner könnten Botensubstanzen des Immunsystems im Blut neutralisiert werden.
Studien
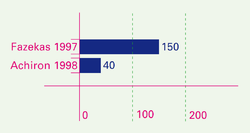
Bereits 1983 erfolgten die ersten Behandlungsversuche von MS mit intravenösen Immunglobulinen (IVIG). Zwei Doppelblindstudien mit insgesamt 190 behandelten Patienten wurden über zwei Jahre durchgeführt und sind die Grundlage der folgenden Darstellung.[2][1] Allerdings unterscheiden sich beide Studien in der Art der Immunglobulingabe: Einmal[1] wurden 200mg/kg Körpergewicht monatlich und einmal[2] 400 mg/kg Körpergewicht alle zwei Monate gegeben.
Wirkungen
In zwei Studien konnte eine deutliche Reduktion der Schubrate gezeigt werden: 24 von 100 Patienten hatten therapiebedingt in zwei Jahren keinen Schub. Ein Effekt auf die Beeinträchtigung war jedoch nicht nachzuweisen. Allerdings war die Schubrate in der Placebogruppe ungewöhnlich hoch. Eine aktuelle Studie zeigt jedoch keine Wirksamkeit von IVIG über ein Jahr Therapie bei Patienten mit geringer Schubaktivität.[3] Auch die richtige Dosierung ist nicht geklärt. Eine Zulassung für IVIG zur MS-Therapie besteht nicht. Hauptendpunkte waren in der Achiron-Studie[2] die jährliche Schubrate und in der Fazekas- Studie[1] die Veränderung der Beeinträchtigung. Zur Vergleichbarkeit der MS-Therapien wird allerdings in dieser Broschüre einheitlich für alle Studien die Anzahl der Patienten ohne Schübe über zwei Jahre dargestellt sowie die Anzahl der Patienten, bei denen die Beeinträchtigung nicht zunimmt. Diese Daten sind auch in einem Cochrane Review analysiert worden.[4]
Anzahl der Patienten mit Schüben innerhalb von zwei Jahren
Bei der Immunglobulintherapie hatten 54 von 100 Patienten keinen Schub in zwei Jahren. In der Placebogruppe waren es 30 von 100 Patienten. Daraus folgt, dass 54 - 30 = 24 von 100 Patienten von der Therapie einen Nutzen haben.
- 24 von 100 Patienten profitieren von der Therapie
- 76 von 100 Patienten haben keinen Nutzen von der Therapie
Wirksamkeit bezogen auf die Zunahme der Beeinträchtigung in zwei Jahren
Um die Zunahme der Beeinträchtigung zu bestimmen, wurde nicht wie bei anderen Studien eine Bestätigung der Verschlechterung in einer zweiten Untersuchung gefordert. So lässt sich diese Studie nicht gleichwertig analysieren. Nur mit Vorsicht lässt sich deshalb errechnen, dass unter IVIG bei 16 von 100 Patienten die Beeinträchtigung in zwei Jahren zunahm. In der Kontrollgruppe war dies bei 21 von 100 Patienten der Fall. Daraus folgt, dass 21 - 16 = 5 von 100 Patienten von der Therapie profitieren.
Weitere Wirkungen
Schubrate
Die Schubrate lag in der Fazekas-Studie[1] bei 0,52 Schüben pro Jahr pro Patient bei mmunglobulintherapie und bei 1,26 bei Einnahme von Placebo. In der Achiron-Studie[2] lag die Schubrate bei 0,59 unter Immunglobulintherapie und bei 1,61 Schüben pro Jahr unter Placebo. Effekte auf die Veränderung der Beeinträchtigung In der Fazekas-Studie[1] verminderte sich im EDSS die Beeinträchtigung bei 23 von 75 Patienten unter IVIG gegenüber 10 von 75 bei Gabe von Placebo. Es kam also zu 23 - 10 = 13 therapiebedingten Verbesserungen. In der Achiron-Studie[2] verminderte sich die Beeinträchtigung bei 5 von 20 Patienten unter IVIG und bei zwei Patienten von 20 unter Placebo. Hier kam es hier also zu 5 - 2 = 3 therapiebedingten Verbesserungen. Im Mittel lag die Beeinträchtigung gemessen auf der EDSS-Skala bei Fazekas unter IVIG bei 3,09 gegenüber 3,49 unter Placebo; bei Achiron bei 2,97 unter Placebo und bei 2,6 unter Immunglobulintherapie, was statistisch kein signifikanter Unterschied ist.
Wirkungen auf das Kernspinbild
Lediglich in der Achiron-Studie wurden Kernspindaten erhoben. Die Gesamtzahl der Entzündungsherde war hier in beiden Gruppen nach Studienende gleich. Eine weitere Untersuchung mit 26 Patienten stellte das Kernspin in den Mittelpunkt.[5] Allerdings fand die Untersuchung nur über sechs Monate statt und die Immunglobulin-Dosierung war mit monatlich zwei Gramm pro Kilogramm Körpergewicht ungewöhnlich hoch. Die Patienten erhielten je drei Monate Placebo und drei Monate IVIG. Hier zeigten sich unter Immunglobulintherapie weniger kontrastmittelspeichernde Entzündungsherde (Glossar) als bei den gleichen Patienten in einer Placebophase. Ähnliches zeigten andere Autoren für 400mg/Kilogramm Körpergewicht bei 7 von 13 Patienten.[6]
Neuere Studie zur Dosisfindung
Eine neuere Studie[7] hat zwei Dosierungen von Immunglobulinen (200mg/kg und 400mg/ kg Körpergewicht) gegen Placebo über ein Jahr verglichen. Hier zeigten beide Dosierungen keine Wirksamkeit. Patienten hatten weniger Krankheitsaktivität als in früheren Studien. Damit ist die Wirksamkeit von Immunglobulinen bei SRMS erneut in Frage gestellt.
Nebenwirkungen
Nebenwirkungen in Form von Hautausschlägen zeigten sich nur bei der Hochdosistherapie mit Immunglobulinen. Es gibt bislang keine Studien, die die Entwicklung der Nebenwirkungen über den Verlauf der gesamten Studie darstellen, so dass der Wirksamkeit nach zwei Jahren nicht die Nebenwirkungen in zwei Jahren gegenübergestellt werden können. Auch allergische Reaktionen müssen nicht zu Beginn, sondern können auch erst im Verlauf auftreten. Patienten der Fazekas-Studie entwickelten einen Hautausschlag, der sich bereits nach wenigen Tagen wieder zurückbildete. In der Achiron-Studie[2] zeigten sich keine der sonst gehäuft unter Immunglobulintherapie auftretenden Nebenwirkungen. In der Hochdosis-Studie von Sörensen[5] fanden sich allerdings gehäuft Hautauschläge bei der Immunglobulintherapie.
Prinzipiell kann die Immunglobulintherapie allergische Reaktionen hervorrufen. Diese können sich mit Kreislaufschwäche, Schwindel, Hautausschlag oder Luftnot äußern. Sehr selten kommt es zu lebensbedrohlichen Zuständen. Bei einem angeborenen Immunglobulin-A-Mangel kann es zu schweren allergischen Reaktionen kommen. Weiterhin kann es durch eine Verdickung des Bluts zu Nierenschäden, Herzinfarkten und Schlaganfällen kommen sowie bei herzschwachen Patienten zu einer Überbelastung des Herzens. Schließlich sind vereinzelt Fälle einer Hirnhautentzündung ohne Erreger (aseptische Meningitis) beschrieben. Als Beschwerden traten Fieber, Kopfschmerzen, Nackensteifigkeit, Lichtempfindlichkeit und Schläfrigkeit auf.
Die Beschwerden waren nach Absetzen der Immunglobulintherapie wieder rückläufig. Zusätzlich besteht das Risiko einer Infektion, da Immunglobuline aus Blutspenden gewonnen werden. Viele Viren werden durch die Reinigung inaktiviert. Aber insbesondere virusbedingte Leberentzündungen (Hepatitis C-Viren) sind vereinzelt unter der Therapie beschrieben. Ein ungelöstes Problem stellt die Reinigung von so genannten Prionen dar, den Erregern des Rinderwahnsinns und der Jakob-Creutzfeld-Erkrankung. Diese können bislang noch nicht inaktiviert werden. Systematische Untersuchungen über Langzeitnebenwirkungen liegen nicht vor.
Wie viele Patienten müssen behandelt werden, damit ein Behandelter einen Nutzen hat?
Um einen Schub in zwei Therapiejahren zu verhindern, müssen vier Patienten mit Immunglobulinen behandelt werden.
Schwächen der Studien zur Immunglobulintherapie
Effekt auf die Zunahme der Beeinträchtigung Der mittlere Unterschied im EDSS nach zwei Jahren Therapie lag bei 0,4 EDSS-Punkten in einem unteren Bereich des EDSS (Placebo 3,49; Immunglobuline 3,09). Dabei veränderte sich auch die Placebogruppe kaum, die Immunglobulingruppe besserte sich geringfügig.
Effekt auf das Kernspin
Insgesamt ist die Datenlage zum Kernspin- Verlauf unter Immunglobulintherapie sehr dürftig. In einer Kurzzeitstudie von Sörensen[5] ließ sich bei sechsmonatiger Hochdosistherapie ein Effekt auf die Anzahl an Kontrastmittelspeicherungen, bestehende und neue Läsionen nachweisen. Bezogen auf das gesamte Ausmaß an nachweisbaren Läsionen zeigte sich hingegen kein solcher Effekt.
Sind Immunglobuline wirksamer als Interferone?
Es gibt bislang keine Studien, die die Wirksamkeit von IVIG, Interferonen und anderen Therapien im direkten Vergleich untersuchen. Die Gegenüberstellung der Studienergebnisse einzelner Therapiestudien ist methodisch problematisch. Auch wurde bis heute keine optimale Dosierung des IVIG dokumentiert. Insgesamt scheint der Effekt vergleichbar zu sein, auch wenn vergleichbare Kernspin-Daten über zwei Jahre Therapieverlauf fehlen. Vorteilhaft gegenüber der Interferontherapie ist sicherlich die nur einmal im Monat notwendige Gabe und die generell gute Verträglichkeit von IVIG.
Häufig gestellte Fragen
Haben Immunglobuline eine heilende Wirkung auf die defekten Myelinscheiden? Laboruntersuchungen hatten 1990 einen möglichen wiederherstellenden (remyelinisierenden) Effekt auf Myelinschäden vermutet. Eine erste Studie schien das zu bestätigen.[8] Weitere Untersuchungen konnten diese Ergebnisse jedoch nicht bestätigen.[9][10] Insofern ist die „reparierende“ Wirkung durch die Immunglobulintherapie als eher gering zu erachten.
Welche Dosis ist die richtige?
In einer Studie über zwölf Monate[11] wurden die Dosierungen von 200 und 400mg pro Kilogramm Körpergewicht verglichen. Über diese kurze Zeit fand sich kein Unterschied der Wirkungen zwischen den Dosierungen. Lediglich in den Kernspinanalysen fand sich ein geringer Vorteil einer höheren Dosis. In einer neuen Dosisfindungsstudie[7] zeigte sich Nutzen der Therapie unabhängig von der Dosierung.
Was passiert, wenn man das Medikament absetzt?
Systematische Untersuchungen zum Absetzen von IVIG gibt es nicht. Dennoch ist eine Zunahme der Krankheitsaktivität nach dem Absetzen der Therapie prinzipiell denkbar.
Wie lange kann man und wie lange muss man das Medikament nehmen?
Da Immunglobuline weder die Erkrankung heilen noch zum Stillstand bringen, müssen sie dauerhaft verabreicht werden. Bei offensichtlicher Verschlechterung der Erkrankung wie bei deutlichen Nebenwirkungen muss überlegt werden, ob ein Absetzen oder ein Medikationswechsel sinnvoll ist.
Können Immunglobuline in der Schwangerschaft oder in der Stillzeit genommen werden?
Prinzipiell ist eine Einnahme während der Schwangerschaft und Stillzeit möglich. Die Schwangerschaft schützt allerdings besser vor Verschlechterungen als die meisten Immuntherapien. Nach der Geburt eines Kindes kann es jedoch gehäuft zu Schüben kommen. Damit könnten IVIG eine Therapie sein, um in der Zeit nach der Geburt eines Kindes zu behandeln. Eine Zulassung von IVIG besteht allerdings nicht. In der GAMPP (Gammaglobulin post Partum) Studie[12] wurden 2 verschiedene Dosierungen von IVIG ab der Geburt für drei Tage und dann monatlich mit 150mg/kg KG über sechs Monate durchgeführt. Die Patientinnen hatten in den sechs Monaten eine Schubhäufigkeit, die ähnlich der Zeit vor der Schwangerschaft war. Angesichts der Tatsache, dass normalerweise die Schubrate deutlich nach der Geburt erhöht ist, wird ein Nutzen der Therapie geschlussfolgert. Ohne Placebogruppe in der Studie ist dieser aber nicht sicher.
Welchen Einfluss hat die Immunglobulin-Therapie auf die Lebensqualität?
Die monatlichen Infusionsgabe und die damit verbundenen Arztbesuche können als Einschränkung der Lebensqualität empfunden werden. Nebenwirkungen sind selten.
Wann dürfen Immunglobuline nicht genommen werden?
Bei einem angeborenen Immunglobulin A-(IgA)-Mangel dürfen Immunglobuline auf keinen Fall genommen werden, da es zu schweren allergischen Reaktionen kommen könnte. Insofern sollte vor Therapiebeginn eine IgA-Bestimmung erfolgen.
Was muss bei der Therapie beachtet werden?
Insbesondere muss eine mögliche Verdickung des Bluts durch die Therapie erkannt werden. Die daraus resultierenden Komplikationen können auch noch Jahre nach der Therapie auftreten.
Wechselwirkungen mit anderen Medikamenten
Wechselwirkungen sind kaum bekannt, da diese Fragestellung bislang kaum erforscht wurde.
Wie erfolgt die Therapie?
Immunglobuline werden als Infusion verabreicht. Generell erfolgt die Gabe einmal monatlich. Dabei schwanken die Dosierungen in den Studien von 200-1.000 mg/pro Kilogramm Körpergewicht je Monat. Die Gabe sollte nicht zu schnell erfolgen, anfangs mit 15 Tropfen/Minute, später mit 50 Tropfen/Minute. Insgesamt dauert die Gabe ein bis zwei Stunden.
Immunglobuline
Im Folgenden sollen die Balken (aus dem Kasten - Kap. 7.6.1. Immunglobuline) ausdifferenziert dargestellt und erklärt werden.
Patienten ohne Zunahme einer Beeinträchtigung
Hier wird die Hauptwirkung auf die Verhinderung der Beeinträchtigungszunahme dargestellt.
Männchen mit Gehstock werden für Zunahme der Beeinträchtigung eingesetzt. Männchen mit Händen auf dem Rücken stehen für Stabilität und Männchen mit Daumen stehen für die Anzahl der Patienten, bei denen ein Medikament wirksam die Zunahme der Beeinträchtigung verhindert. Die Werte erscheinen auf 100 Patienten bezogen. Dargestellt werden:
1. Patienten, die trotz des Medikaments eine Zunahme der Beeinträchtigung erfahren,
2. Patienten, die durch das Medikament bedingt keine Zunahme der Beeinträchtigung erfahren,
3. Patienten, die auch ohne Medikament keine Zunahme der Beeinträchtigung erfahren hätten.
Die Ergebnisse können wie gerade beschrieben dargestellt werden. In einer anderen Darstellungsweise können die unterschiedlichen Therapiegruppen einer Studie getrennt (entweder Placebo- oder Verumgruppe) darstellt werden.
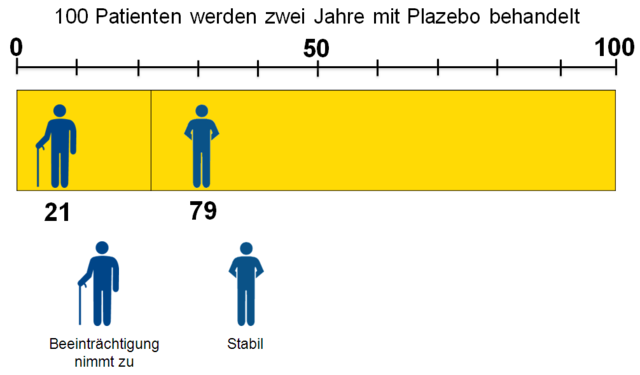
Placebogruppe
Für die Patienten der Studie, die mit Placebo behandelt wurden, sähe die Darstellung so aus:
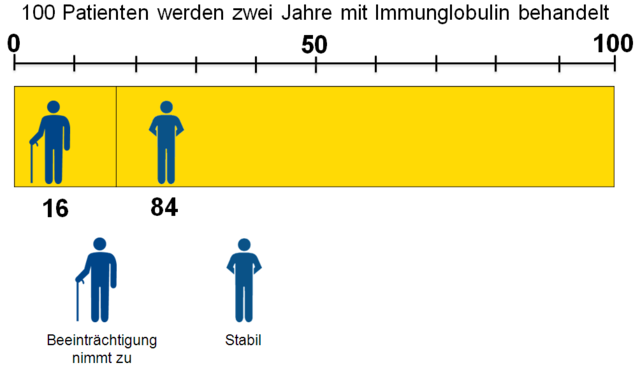
Verumgruppe
Für die Patienten, die mit Immunglobulin behandelt werden, sähe dann die Darstellung so aus:
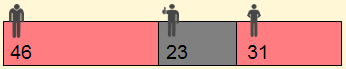
Nutzen durch das Medikament
Statt 21 Patienten haben jetzt nur 16 Patienten eine Zunahme der Beeinträchtigung oder anders gesagt: statt 79 Patienten bleiben nun 84 Patienten stabil.
Wenn nun dargestellt werden soll, wie viele Patienten einen Nutzen durch die Therapie haben, muss berechnet werden, wie viele Patienten zusätzlich zur Behandlung mit Placebo stabil bleiben. Oder anders gesagt, wie viele Patienten weniger eine Zunahme der Beeinträchtigung haben.
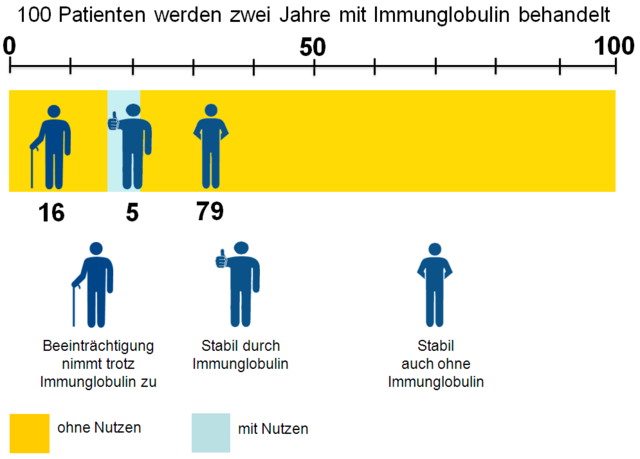
So entsteht die von uns eingesetzte zusammenfassende Grafik:
Für die obige Grafik heißt dies, dass auf 100 Patienten gerechnet:
- 16 Patienten trotz der Immunglobulin-Therapie eine Zunahme der Beeinträchtigung hatten,
- 5 Patienten bedingt durch die Therapie keine Zunahme der Beeinträchtigung hatten,
- 79 Patienten unabhängig von der Therapie keine Zunahme der Beeinträchtigung hatten.
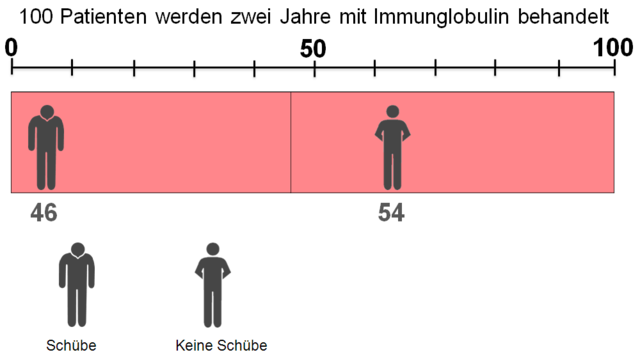
Patienten mit Schubfreiheit
Im Folgenden sollen die Balken (aus dem Kasten) ausdifferenziert dargestellt und erklärt werden. Hier wird die Hauptwirkung auf die Schubfreiheit dargestellt.
Männchen mit "hängendem" Kopf werden für das Auftreten von Schüben genutzt. Männchen mit Händen auf dem Rücken stehen für Stabilität und Männchen mit Daumen stehen für die Anzahl der Patienten, bei denen ein Medikament wirksam das Auftreten von Schüben verhindert. Die Werte erscheinen auf 100 Patienten bezogen. Dargestellt werden:
1. Patienten, die trotz des Medikaments einen oder mehrere Schübe erleiden,
2. Patienten, die durch das Medikament bedingt keine Schübe erleiden,
3. Patienten, die auch ohne Medikament keine Schübe erlitten hätten.
Die Ergebnisse können wie gerade beschrieben dargestellt werden. In einer anderen Darstellungsweise können die unterschiedlichen Therapiegruppen einer Studie getrennt (entweder Placebo- oder Verumgruppe) darstellt werden.
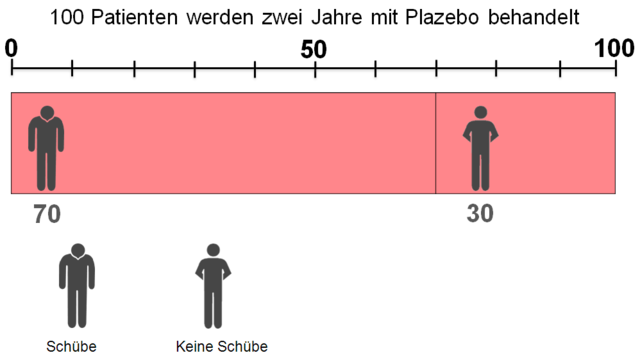
Placebogruppe
Für die Patienten der Studie, die mit Placebo behandelt wurden, sähe die Darstellung so aus:
Verumgruppe
Für die Patienten, die mit Immunglobulin behandelt werden, sähe dann die Darstellung so aus:
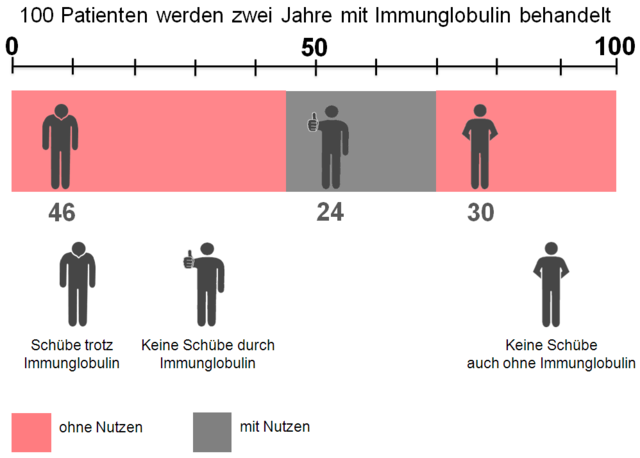
Nutzen durch das Medikament
Statt 70 Patienten erleiden jetzt nur 46 Patienten einen Schub oder anders gesagt: statt 30 Patienten bleiben nun 54 Patienten schubfrei.
Wenn nun dargestellt werden soll, wie viele Patienten einen Nutzen durch die Therapie haben, muss berechnet werden, wie viele Patienten zusätzlich zur Behandlung mit Placebo schubfrei bleiben. Oder anders gesagt, wie viele Patienten weniger einen Schub erleiden.
So entsteht die von uns eingesetzte zusammenfassende Grafik:
Für die obige Grafik heißt dies, dass auf 100 Patienten gerechnet:
- 46 Patienten trotz der Immunglobulin-Therapie einen oder mehrere Schübe erlitten,
- 24 Patienten bedingt durch die Therapie keine Schübe erlitten,
- 30 Patienten unabhängig von der Therapie keine Schübe erlitten hatten.
Linolensäure
Einige Studien sprechen für eine geringere Beeinträchtigungszunahme bei Zufuhr von Linolensäuren oder ähnlichen Substanzen, insbesondere in frühen Phasen der Erkrankung. Die Befunde sind jedoch nicht statistisch gesichert.[13]
Wirkungen
In der Studie von Bates[14] 1989 wurden Fischölkapseln mit zwei anderen ungesättigten Fettsäuren verwandt (s.u.). In den Studien von Bates[14] und Millar[15] bei SRMS waren in der Therapiegruppe die Schübe kürzer und leichter. In der Studie von Paty[16] wurden auch Patienten mit chronisch-progredientem Verlauf eingeschlossen. Hier zeigte sich kein Effekt. Diese Studien wurde von Dworkin[17] zusammenfassend analysiert. Bei insgesamt 181 Patienten fand sich während einer zweijährigen Beobachtungszeit eine um 0,29 EDSS-Punkte geringere Zunahme der Beeinträchtigung unter Linolensäure. Dieser Effekt war statistisch nicht signifikant. In der Placebogruppe gab es vier schubfreie Patienten mehr. Auch dieses Ergebnis war nicht statistisch sicher. Allerdings waren unter Linolensäure die Schübe schwächer. 1989 wurde von Bates eine weitere Studie mit einem Abkömmling der Linolensäure durchgeführt[18], in der auch in Fischölkapseln enthalten war. Die Patienten erhielten 20 Kapseln mit je 500 mg Fischöl täglich, was 1,7 g Eicosapentaensäure und 1,1 g Docosahexaensäure täglich entspricht. In der Studie wurden über zwei Jahre 312 Patienten mit schubförmiger MS mit einem Schub innerhalb der letzten zwei Jahre untersucht. Hier zeigten 45% unter Linolensäure (66 von 145) und 55% (82 von 147) unter Placebo eine Beeinträchtigungszunahme im EDSS. Damit profitieren 10 von 100 (VB: -1 -22) Patienten von der Therapie.
Das Ergebnis war aber statistisch nicht signifikant, sondern zeigte nur einen Trend auf. Bei einer Subgruppenanalyse der geringer beeinträchtigten Patienten konnte in dieser Studie ebenfalls nur ein Trend nachgewiesen werden, der auch für die Parameter Schubrate, Schubschwere und Schubdauer galt.
Nebenwirkungen
(Text folgt)
Schwächen der Studien zur Linolensäure-Therapie
Sämtliche Linolensäurestudien sind nicht nach heutigen Studienstandards konzipiert. Insofern müssen die Ergebnisse mit Vorsicht bewertet werden. Am ehesten erfüllt die Studie von Bates1 moderne Standards. In ihr wurden ausreichend viele Patienten untersucht. Allerdings gab es in dieser Studie keine echte Placebogruppe, da diese Patienten im Gegensatz zur Linolensäuregruppe eine Diätberatung erhielten. Es ist somit möglich, dass der Nutzen der Therapie durch die Wirkung der Diätberatung auf die Ernährungsgewohnheiten in der Placebogruppe verdeckt wurde. So genannte Subgruppenanalysen wie in den Linolensäurestudien für geringer beeinträchtigte Patienten werden oft benutzt, um im Nachhinein noch ein positives Ergebnis für eine Teilgruppe zu finden. Insofern sind sie mit Vorsicht zu bewerten.
Das Ergebnis war aber statistisch nicht signifikant, sondern zeigte nur einen Trend auf. Bei einer Subgruppenanalyse der geringer beeinträchtigten Patienten konnte in dieser Studie ebenfalls nur ein Trend nachgewiesen werden, der auch für die Parameter Schubrate, Schubschwere und Schubdauer galt.
Kortison
(Text folgt)
Wirkungen
(Text folgt)
Nebenwirkungen
(Text folgt)
Cyclophosphamid
(Text folgt)
Studien
Gezielte Studien zur SRMS gibt es nicht.
Wirkungen
(Text folgt)
Nebenwirkungen
Angesichts der Nebenwirkungen (Nebenwirkungen bei schubförmiger MS) kann dieses Therapiekonzept nur in Einzelfällen bei sehr hoher Schubaktivität mit erheblichen Beeinträchtigungen diskutiert werden.
Keine Immuntherapie
Systematische Daten liegen zu der Option, keine Therapie zu beginnen nicht vor. Dennoch lassen sich aus den Placebogruppen der Therapiestudien Schlußfolgerungen ziehen. So finden sich über zwei Jahre bei den Interferontherapiestudien in den Placbogruppen 29 von 100 Patienten mit Zunahme einer Beeinträchtigung. Bei 69 von 100 Patienten tritt mindestens ein zweiter Schub auf.
Kombinationstherapien
(Text folgt)
Studien
Möglicherweise haben Patienten einen Nutzen durch die kombinierte Behandlung mit Azathioprin und Interferon-ß.[23] Die bisher vorliegenden Daten sprechen für die Verträglichkeit einer solchen Therapie. Eine Aussage über den Nutzen dieser Kombinationstherapie lässt sich jedoch aus den Studienergebnissen nicht ableiten.
Wirkungen
(Text folgt)
Nebenwirkungen
(Text folgt)
Alternative, komplementäre und Nahrungsergänzungstherapien
Keine Studie hat bislang eine klare Evidenz für eine der so genannten Alternativtherapien gezeigt. Es gibt einigen Anhalt für einen Effekt der Linolensäuregabe, weshalb diese auch bei den Therapiemöglichkeiten der einzelnen Verlaufsformen Erwähnung findet.
Zahlreiche Untersuchungen haben gezeigt, dass eine große Diskrepanz zwischen der Anwendung von Alternativtherapien und ihrer wissenschaftlichen Fundierung besteht. Im Folgenden sollen kurz die Ansätze, für die zumindest einige Daten vorliegen, referiert werden.
Vitamin C, Vitamin A, Selen
Als Antioxidantien könnten diese Substanzen einen Effekt bei MS haben. Klinische Studien liegen derzeit jedoch nicht vor, nur einige Hinweise aus Tierversuchen.
Vitamin D
Vitamin D wirkt möglicherweise immunmodulierend (Glossar). In Tierversuchen gibt es Hinweise für einen Nutzen bei einer der MS ähnlichen Erkrankung. Klinische Studien stehen aus. Eine neue Untersuchung bei 200.000 Krankenschwestern in den USA zeigt, dass die Einnahme von Vitamin-D möglicherweise vor der Entwicklung einer MS schützt.[24] Ob auch eine therapeutische Wirksamkeit besteht, muss offen bleiben.
Enzymtherapie
Siehe Enzymtherapie unter Therapie ohne Wirksamkeitsnachweis
Fischöl
Siehe oben
Sauerstoffüberdrucktherapie
Sauerstoffüberdrucktherapie ist in verschiedenen Studien untersucht worden. Eine Metaanalyse[25] hat die Ergebnisse zusammengefasst. Ein langfristiger Nutzen kann hier nicht nachgewiesen werden. Im Gegenteil zeigt die größte kontrollierte Studie[26] sogar einen eher negativen Einfluss auf die Leitungsfähigkeit des Sehnervs.
Feldenkrais und Massage
Diese (physiotherapeutischen) Methoden wirken sich positiv auf depressive Verstimmung, Ängstlichkeit und vermindertes Selbstwertgefühl aus.[27] Hinweise für eine positive Beeinflussung des Erkrankungsverlaufs liegen derzeit nicht vor.
Magnetfeldtherapie, Fußreflexzonenmassage und Neuraltherapie
Diese Methoden scheinen Symptome wie Spastik und Blasenstörungen kurzzeitig positiv zu beeinflussen.[27] Hinweise für eine Beeinflussung des Erkrankungsverlaufs gibt es nicht.
Cannabis
Nachdem einige kleine Untersuchungen widersprüchliche Ergebnisse erbracht hatten, zeigte eine Doppelblindstudie (Glossar) mit insgesamt 667 Patienten, dass Cannabis die subjektive Beeinträchtigung durch Spastik und Schmerzen mindert. In objektiven Messungen der Spastik konnte jedoch keine Verbesserung belegt werden.[28] Hinweise für eine Beeinflussung des Erkrankungsverlaufs gibt es nicht.
Yoga
Eine Studie zeigte bei 57 Patienten, die über sechs Monate an einer Yoga-Therapie teilnahmen, eine Besserung von MS-bedingter Müdigkeit, aber keine Veränderung in anderen Bereichen der Lebensqualität, der Stimmung oder geistiger Funktionen.[29]
Olivenöl
Inhaltssubstanzen des Olivenöls könnten antientzündliche aber auch nervenschützende Wirkungen bei MS haben. Dies ist bislang nur im Tierversuch belegt.
Sport
Bislang gibt es kaum Untersuchungen zu den biologischen Wirkungen von Sport bei MS. Ein Nutzen auf Lebensqualität und einzelne Beschwerden ist in einer Metaanalyse belegt.[30] Aus Untersuchungen zu Sport und Immunsystem und Untersuchungen mit alten Menschen finden sich jedoch Hinweise, dass Sport sowohl das Immunsystem moduliert als auch möglicherweise Reparatur im Nervensystem fördert.
Stressmanagement
Lange besteht eine wissenschaftliche Diskussion, ob Stressbelastungen den Ausbruch einer MS als auch das Auftreten von Schüben der Erkrankung mit beeinflussen. Eine Metaanalyse[31] kommt zu dem Schluss, dass die Mehrzahl der Studien für einen solchen Zusammenhang spricht. Insofern erscheinen Stressmanagement und Bearbeitung psychischer Belastungen sinnvoll, wenngleich bislang keine Studie den möglichen positiven Effekt solcher Maßnahmen auf den Verlauf untersucht hat.
Einzelnachweise
- ↑ 1,0 1,1 1,2 1,3 1,4 1,5 Fazekas F et al. Randomised placebo-controlled trial of monthly intravenous immunoglobulin therapy in relapsing-remitting multiple sclerosis. Austrian Immunoglobulin in Multiple Sclerosis Study Group. Lancet 1997; 349:589-93.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 2,6 Achiron et al. Intravenous immunoglobulin treatment in multiple sclerosis. Effect on relapses. Neurology 1998; 50:398-402.
- ↑ Fazekas F et al. Intravenous immunoglobulin in relapsing-remitting multiple sclerosis: A dose-finding trial. Neurology 2008; 71:265-271.
- ↑ Gray O et al. Intravenous immunoglobulins for multiple sclerosis. Cochrane Database Syst Rev 2003; CD002936.
- ↑ 5,0 5,1 5,2 Sorensen PS et al. Intravenous immunoglobulin G reduces MRI activity in relapsing multiple sclerosis. Neurology 1998; 50:1273-81.
- ↑ Teksam M et al. Qualitative and quantitative volumetric evaluation of the efficacy of intravenous immunoglobulin in multiple sclerosis: preliminary report. Neuroradiology 2000; 42:885-9.
- ↑ 7,0 7,1 Fazekas F et al. Intravenous immunoglobulin in relapsing-remitting multiple sclerosis: a dose-finding trial. Neurology 2008; 71(4):265-71.
- ↑ van Engelen BG et al.Improved vision after intravenous immunoglobulin in stable demyelinating optic neuritis. Ann Neurol 1992; 32:834-5.
- ↑ Stangel M et al. Placebo controlled pilot trial to study the remyelinating potential of intravenous immunoglobulins in multiple sclerosis. J Neurol Neurosurg Psychiatry 2000; 68:89-92.
- ↑ Noseworthy JH et al. A randomized trial of intravenous immunoglobulin in inflammatory demyelinating optic neuritis. Neurology 2001; 56:1514-22.
- ↑ Lewanska M et al. No difference in efficacy of two different doses of intravenous immunoglobulins in MS: clinical and MRI assessment. Eur J Neurol 2002; 9:565-72.
- ↑ Haas J et al. A dose comparison study of IVIG in postpartum relapsing-remitting multiple sclerosis. Mult Scler 2007; 13:900-8.
- ↑ Richards RG A review of the natural history and epidemiology of multiple sclerosis: implications for resource allocation and health economic models. Health Technol Assess 2002; 6:1-73.
- ↑ 14,0 14,1 14,2 Bates D et al. Polyunsaturated fatty acids in treatment of acute remitting multiple sclerosis. BMJ 1978; 2:1390-1.
- ↑ 15,0 15,1 Millar JH et al.Double-blind trial of linoleate supplementation of the diet in multiple sclerosis. BMJ1973; 1:765-8.
- ↑ 16,0 16,1 Paty DW. Double-blind trial of linoleic acid in multiple sclerosis.Arch Neurol 1983; 40:693-4.
- ↑ 17,0 17,1 Dworkin RH et al. Linoleic acid and multiple sclerosis: a reanalysis of three double-blind trials. Neurology 1984; 34:1441-5.
- ↑ Bates D et al. A double-blind controlled trial of longchain n-3 polyunsaturated fatty acids in the treatment of multiple sclerosis. J Neurol Neurosurg Psychiatry 1989; 52:18-22.
- ↑ Ciccone A et al.Corticosteroids for the long-term treatment in multiple sclerosis. Cochrane Database Syst Rev 2008; CD006264.
- ↑ Miller H et al. Multiple sclerosis. Trials of maintenance treatment with prednisolone and soluble aspirin. Lancet 1961; 1:127–9.
- ↑ Ciccone A et al. Periodic intravenous methylprednisolone megadoses to prevent relapses in multiple sclerosis [Boli steroidei Preventivi per la Sclerosi Multipla (BPSM)]. Protocol approved by local Ethics Committee (Ospedale “Valduce”, Como, Italy) 1995.(BPSMGroup)
- ↑ Zivadinov R et al. Effects of IV methylprednisolone on brain atrophy in relapsing-remitting MS. Neurology 2001; 57:1239-47.
- ↑ Lus G et al. Azathioprine and interferon beta(1a) in relapsing-remitting multiple sclerosis patients: increasing efficacy of combined treatment. Eur Neurol 2004; 51:15-20.
- ↑ Munger KL et al. Vitamin D intake and incidence of multiple sclerosis. Neurology 2004; 62:60-5.
- ↑ Bennett M et al. Treatment of multiple sclerosis with hyperbaric oxygen therapy. Undersea Hyperb Med 2001; 28:117-22.
- ↑ Barnes MP et al. Hyperbaric oxygen and multiple sclerosis: final results of a placebo-controlled, double-blind trial. J Neurol Neurosurg Psychiatry 1987; 50:1402-6.
- ↑ 27,0 27,1 Huntley A et al. Complementary and alternative therapies for treating multiple sclerosis symptoms: a systematic review. Complement Ther Med 2000; 8:97-105.
- ↑ Zajicek J et al. Cannabinoids for treatment of spasticity and other symptoms related to multiple sclerosis (CAMS study): multicentre randomised placebo-controlled trial. Lancet 2003; 362:1517-26.
- ↑ Oken BS et al. Randomized controlled trial of yoga and exercise in multiple sclerosis. Neurology 2004; 62:2058-64.
- ↑ Motl RW et al. Effect of exercise training on quality of life in multiple sclerosis: a meta-analysis. Mult Scler 2008; 14(1):129-35.
- ↑ Mohr DC et al. Association between stressful life events and exacerbation in multiple sclerosis: a meta-analysis. BMJ 2004; 328:73.