Im Folgenden sind die Wirkungen auf der Basis der Studie AFFIRM[57] dargestellt.
1. Wirkung auf die Schubfreiheit
Die Grafik am Kapitelanfang zeigt, wie viele Patienten nach 2 Jahren Therapie mit Natalizumab oder Einnahme von Placebo noch schubfrei waren. Daraus lässt sich der absolute Nutzen (absolute Risikoreduktion) und der relative Nutzen (relative Risikoreduktion) berechnen.
Hier wird die Anzahl der Patienten mit Schüben beschrieben. Um Studienergebnisse mit unterschiedlichen Teilnehmerzahlen besser vergleichen zu können, werden die Ergebnisse bezogen auf 100 Patienten dargestellt:
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl der Patienten mit Schüben bei Natalizumab-Gabe (28) von denen bei Placebo (54) abzieht. Hier profitieren 54 – 28, also 26 von 100 Patienten von der Therapie. Das entspricht dem absoluten Nutzen (oder auch der absoluten Risikoreduktion).
- 26 von 100 Patienten haben einen Nutzen von der Therapie.
- 28 von 100 Patienten profitieren nicht von der Therapie, da sie trotz der Einnahme von Natalizumab einen Schub hatten.
- 46 von 100 Patienten profitieren nicht, da sie auch ohne Natalizumab schubfrei geblieben sind.
2. Wirkung auf die Anzahl der Schübe pro Jahr
Die jährliche Schubrate zeigt, wie viele Schübe durchschnittlich pro Jahr pro Patient auftraten. Sie lag in der Placebo-Gruppe bei 0,73 Schüben gegenüber 0,23 in der Natalizumab-Gruppe. Etwas verständlicher ausgedrückt: Die Patienten in der Placebo-Gruppe haben im Durchschnitt alle 1,4 Jahre einen Schub, die Patienten in der Natalizumab-Gruppe nur alle 4,3 Jahre.
3. Wirkung auf die Zunahme der Behinderung
Die Zunahme der Behinderung wurde in den Zulassungsstudien mit Hilfe des EDSS gemessen, einer Behinderungsskala von 0 bis 10 (wobei 0 keiner Behinderung, 10 Tod entspricht).
Die Grafik am Kapitelanfang zeigt, wie viele Patienten nach 2 Jahren Therapie mit Natalizumab oder Gabe von Placebo keine Zunahme der Behinderung hatten. Dargestellt ist wieder der absolute Nutzen (absolute Risikoreduktion) und der relative Nutzen (relative Risikoreduktion).
Im Glossar finden Sie Angaben zum Nutzen von Medikamenten bei anderen Erkrankungen. So bekommen Sie einen Eindruck davon, wie groß die Therapieeffekte bei MS im Vergleich zu denen bei anderen Krankheiten sind.
Im Folgenden wird die Entwicklung der Behinderung in zwei Jahren beschrieben, jeweils bezogen auf 100 Patienten:
- 17 von 100 Patienten haben trotz der Natalizumab-Therapie eine Zunahme der Behinderung.
- 71 von 100 Patienten profitieren nicht von der Therapie, sie haben unabhängig von der Therapie keine Zunahme der Behinderung.
- 12 von 100 Patienten haben durch die Einnahme von Natalizumab keine Zunahme der Behinderung.
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl von Patienten mit einer Behinderungszunahme in der Natalizumab-Gruppe (17) von denen in der Placebo-Gruppe (29) abzieht. Hier profitieren 29 – 17, also 12 von 100 Patienten von der Therapie. Das entspricht dem absoluten Nutzen (oder auch der absoluten Risikoreduktion).
Wirkungen bei sekundär progredienter MS
Die 2018 veröffentlichte ASCEND-Studie (Verlinkung) zur Therapie der sekundär-chronisch progredienten MS (SPMS) konnte keine überzeugende Wirksamkeit von Natalizumab nachweisen. Eine Anwendung im Bereich SPMS ist somit bei bisherigem Datenstand nicht indiziert.
4. Wirkung auf die MRT in zwei Jahren
In der MRT treten Kontrastmittelanreicherungen und so genannte T2-Herde auf, die als Ausdruck der Entzündung bei MS betrachtet werden. Dabei können Herde größer werden oder ganz neu auftreten.
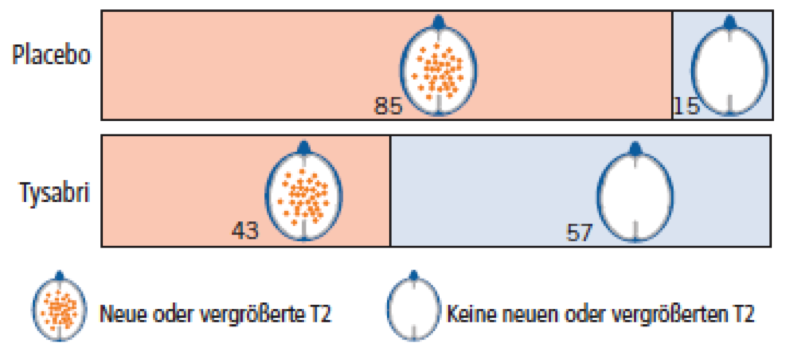
15% der Patienten in der Placebo-Gruppe und 57% in der Natalizumab-Gruppe waren über die Studiendauer frei von neuen oder vergrößerten T2-Herden.
72% der Patienten in der Placebo-Gruppe und 97% in der Natalizumab-Gruppe hatten über die Studiendauer keine Herde mit Kontrastmittelanreicherungen.
Da Kontrastmittelanreicherungen nur eine Momentaufnahme sind, stellen wir nur die Entwicklung der T2-Herde im Querschnitt eines Gehirns grafisch dar. Dargestellt ist die Anzahl von 100 Patienten ohne bzw. mit neuen oder vergrößerten Herden.
Im Glossar finden Sie außerdem Daten zu dem Anteil der Patienten, bei denen es über 2 Jahre keine Anzeichen einer Krankheitsaktivität gab ("NEDA - no evidence of disease activity").
Zulassungsstudien
Zulassungsstudien AFFIRM und SENTINEL:
Die Wirkung von Natalizumab auf die Schubrate und die Zunahme der Behinderung wurde in 2 Zulassungsstudien (AFFIRM[57] und SENTINEL[58]) geprüft und die Ergebnisse im Jahr 2006 veröffentlicht. Insgesamt wurden 2113 Patienten mit schubförmiger MS über einen Zeitraum von 2 Jahren untersucht. Eingeschlossen wurden Patienten, die im Jahr vor Studienbeginn mindestens einen Schub hatten.
- In AFFIRM (Natalizumab Safety and Efficacy in Relapsing Remitting Multiple Sclerosis)[57] wurde Natalizumab gegen Placebo geprüft.
Eingeschlossen wurden 942 Betroffene mit schubförmiger MS und mindestens einem Schub im letzten Jahr. Nicht teilnehmen konnten Patienten, die in den 6 Monaten vor Studienbeginn ein Immunmedikament erhalten oder eine mindestens sechsmonatige Immuntherapie durchgeführt hatten. Die Teilnehmer erhielten alle vier Wochen eine Infusion. 627 Teilnehmer erhielten jeweils 300mg Tysabri®, 315 Teilnehmer ein Placebo. - In SENTINEL (Safety and Efficacy of Natalizumab in Combination with Interferon-β-1a in Patients with Relapsing-Remitting Multiple Sclerosis)[58] mussten Patienten darüber hinaus zuvor mindestens 1 Jahr mit einem Interferon behandelt worden sein und unter dieser Therapie einen Schub entwickelt haben, d.h. sie sprachen auf die Interferontherapie nicht ausreichend an. In dieser Studie wurde dann der Hälfte der Patienten zusätzlich zu Interferon-beta1a Natalizumab gegeben, die andere erhielt nur Interferon-beta 1A. Diese Kombination führte jedoch nicht zu einer Zulassung der kombinierten Therapie. Diese Studienergebnisse sind somit für aktuelle Therapieentscheidungen nur begrenzt relevant und werden im Folgenden nicht detailliert beschrieben. Eine PML trat nur in der Verlängerungsphase der SENTINEL-Studie auf. Bei zwei von 589 Patienten in der Gruppe, die Interferon-beta 1a und Natalizumab erhielten, entwickelte sich eine schwere Entzündung des Gehirns (Progressive Multifokale Leukenzephalopathie, PML). Ein Patient überlebte die Infektion mit schweren bleibenden Beeinträchtigungen, eine Patientin verstarb an der PML, die erst nach Ende der zweijährigen Studiendauer aufgetreten war. Nach Bekanntwerden der beiden PML-Fälle wurden die Studien gestoppt und der Vertrieb des Medikaments 2005 vorläufig eingestellt. 2007 wurde Natalizumab wieder vermarktet, die Entwicklung der PML-Fälle wird beobachtet.
