Es existieren zwölf zugelassene Medikamente zur Behandlung der schubförmigen MS. Mit einem Klick auf den jeweiligen Medikamentennamen gelangen Sie direkt zum Kapitel des gewünschten Medikaments.
Seit 2014 werden in den Therapieleitlinien der Deutschen Gesellschaft für Neurologie [3] zwei Gruppen von Immuntherapien unterschieden: Immuntherapien für milde bis moderate Krankheitsverläufe (oft auch Basistherapie genannt) und Immuntherapien für aktive bis hoch aktive Krankheitsverläufe (auch Eskalationstherapie genannt).
Diese Unterteilung versucht zu berücksichtigen, welche Medikamente für welche Patientengruppen von den entsprechenden Behörden zugelassen sind, und wie das Risikoprofil in Abwägung zu dem erwarteten Nutzen einzuschätzen ist. Für milde bis moderate Krankheitsverläufe (Basistherapie) werden eingesetzt:
- Interferone (Avonex®, Betaferon®, Rebif®, Extavia®)
- Glatirameracetat (Copaxone®)
- Teriflunomid (Aubagio®)
- Dimethylfumarat (Tecfidera®).
Für aktive bis hochaktive Krankheitsverläufe (Eskalationstherapie) sind zugelassen:
- Fingolimod (Gilenya®)
- Ozanimod (Zeposia®)
- Natalizumab (Tysabri®)
- Ocrelizumab (Ocrevus®)
- Cladribin (Mavenclad®)
obwohl diese nie als Eskalationstherapie geprüft wurden.
Folgende Medikamente sind als Reservemedikamente zugelassen:
- Alemtuzumab (Lemtrada®)
Von den sechs „Eskalationstherapien“ ist Alemtuzumab "bei aktiver MS" zugelassen. Es ist als einziges Medikament in der Eskalationstherapie geprüft worden. Dies bedeutet, dass es bei einer Patientengruppe eingesetzt wurde, bei denen eine andere Therapie nicht ausreichend gewirkt hatte. Zum anderen wurde bei Lemtrada in den Zulassungsstudien ein direkter Vergleich mit einem Medikament der Basistherapie (Interferon ß1 a) durchgeführt.
Alle anderen aufgeführten Substanzen wurden in den Zulassungsstudien direkt nur gegen ein Placebo (Scheinmedikament) verglichen.
Grundsätzlich lassen sich Medikamente nur vergleichen, wenn sie direkt in einer Studie gegeneinander untersucht wurden. Solche Daten liegen nur für Copaxone® und Interferone sowie für Rebif® und Lemtrada® vor. Dennoch kann eine Übersicht helfen, die unterschiedlichen Wirkungen abzuschätzen.
Darstellung der Therapieeffekte nach absoluter Risikoreduktion am Beispiel des Medikaments Dimethylfumarat (Tecfidera®)
Um die nachfolgende Darstellung zu verstehen, ist es wichtig, zu wissen, dass Studienergebnisse als sogenannte Risikoreduktionen berichtet werden. Dabei werden zwei Formen verwendet, die jeweils unterschiedliche Informationen liefern: die absoute Risikoreduktion (ARR) und die relative Risikoreduktion (RRR).
Die Abbildung zeigt die Anzahl der Patienten mit und ohne Schübe in den beiden Studiengruppen (erster und zweiter Balken), also in der Placebo- und der Fumarat-Gruppe.
Im Zusammenfassungsbalken „Nutzen“ sieht man in Grün die Anzahl der Patienten von 100 mit Fumarat behandelten, die einen Nutzen von der Therapie haben.
Dazu vergleicht man die Patienten mit Schüben unter Placebo mit denen mit Schüben unter Fumarat. Da nur 28 statt 44 Schübe hatten, ist die absolute Risikoreduktion 44 - 28 = 16.
Dagegen haben 56 Patienten unter Fumarat keinen Nutzen, weil sie unabhängig von der Therapie stabil geblieben sind.
Im Folgenden wird nur noch der Zusammenfassungsbalken dargestellt, auch um die Medikamente nebeneinander zu stellen. Wenn Sie im Kapitel des jeweiligen Medikaments auf die Überschriften der einzelnen Balken klicken, finden Sie jedoch alle Zusammenfassungsbalken noch einmal aufgeschlüsselt in ihre Teilbalken, begleitet von Erklärungen. 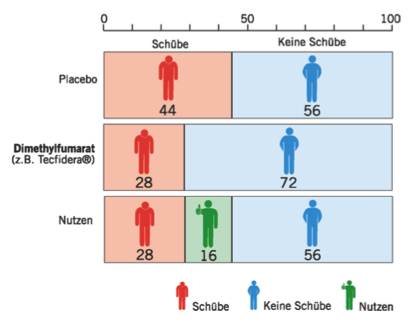
Die folgenden Zahlen gelten für die Therapiestudienergebnisse über 2 Jahre:
- Bei Behandlung mit Interferonen haben 15 von 100 Patienten therapiebedingt keinen Schub in zwei Jahren und 9 von 100 Patienten therapiebedingt keine Zunahme der Beeinträchtigung.
- Unter Copaxone® sind diese Zahlen 10 von 100 für die Schubfreiheit und 7 von 100 für die Verhinderung einer Beeinträchtigungszunahme.
- Unter Tecfidera® sind 16 von 100 Patienten schubfrei und 8 von 100 Patienten haben keine Zunahme der Beeinträchtigung.
- Unter Aubagio® haben 11 von 100 therapiebedingt keinen Schub und 5 keine Zunahme der Beeinträchtigung.
- Unter Gilenya® sind dies 25 von 100 ohne Schub und 7 ohne Beeinträchtigungszunahme.
- Bei Behandlung mit Tysabri® haben 26 von 100 therapiebedingt keinen neuen Schub und 12 keine Zunahme der Beeinträchtigung.
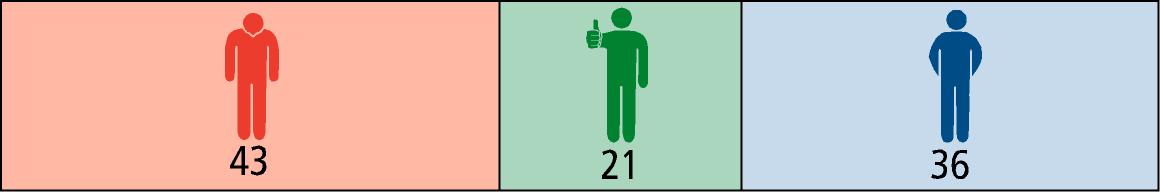
- Unter Mitoxantron® waren 21 von 100 Patienten schubfrei und 14 von 100 Patienten hatten keine Zunahme der Beeinträchtigung.
- Bei Therapie mit Lemtrada® in der Eskalation sind 19 von 100 therapiebedingt schubfrei und 7 von 100 therapiebedingt ohne Zunahme der Beeinträchtigung.
- Unter Cladribin haben 19 von 100 Patienten therapiebedingt keinen Schub in zwei Jahren und 7 von 100 Patienten therapiebedingt keine Zunahme der Beeinträchtigung.
- Bei Behandlung mit Lemtrada® sind 18 von 100 Patienten therapiebedingt schubfrei und 7 von 100 Patienten haben therapiebedingt keine Zunahme der Beeinträchtigung.
Zusammengefasst sind unter der Basistherapie 10-20 von 100 Patienten schubfrei und 7-10 von 100 Patienten progressionsfrei.
Unter Gilenya®, Tysabri® und Mitoxantron® sind dies 21 - 26 von jeweils 100 Patienten schubfrei sowie 7 - 14 von jeweils 100 Patienten progressionsfrei.
Mit der Eskalationstherapie unter Lemtrada® sind 19 von 100 Patienten schubfrei und 7 von 100 Patienten progressionsfrei.
Diese Zahlen sind grafisch in der Tabelle (s.u.) aufgeführt. Alemtuzumab wird in dieser Auflistung zuletzt genannt, das es nur im Vergleich zu Rebif® und nicht im Vergleich zu Placebo untersucht wurde.
Wirkungsvergleich der zugelassenen Immunmedikamente zur Therapie der schubförmigen MS
| Wirkstoff (Handelsname) | Patienten ohne Zunahme der Behinderung | Patienten mit Schubfreiheit |
| Im Vergleich zu Placebo | ||
| Beta-Interferon (z.B. Betaferon®, Avonex®, Rebif®) |
 |
 |
| Peginterferon β-1a (Plegridy®) |
Es erfolgt keine grafische Darstellung der Ergebnisse, da die Studiendauer nur ein Jahr betrug. 4 von 100 Patienten profitieren von der Therapie. |
10 von 100 Patienten profitieren von der Therapie. |
| Glatirameracetat (Copaxone®)*1 |
 |
 |
|
Glatirameracetat 40mg/ml (Copaxone®40) |
Es gab keine signifikanten Unterschiede zwischen den Gruppen hinsichtlich einer Zunahme der Behinderung. |
Es gab keine signifikanten Unterschiede zwischen den Gruppen hinsichtlich der Schubfreiheit. |
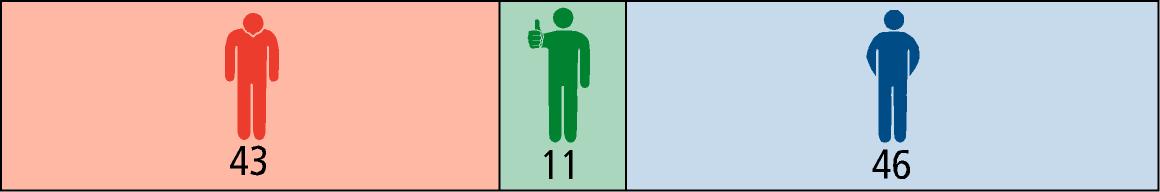
| Dimethylfumarat BG12 (Tecfidera®) |
 |
 |
| Teriflunomid (Aubagio®) |
 |
 |
| Fingolimod (Gilenya®) |
 |
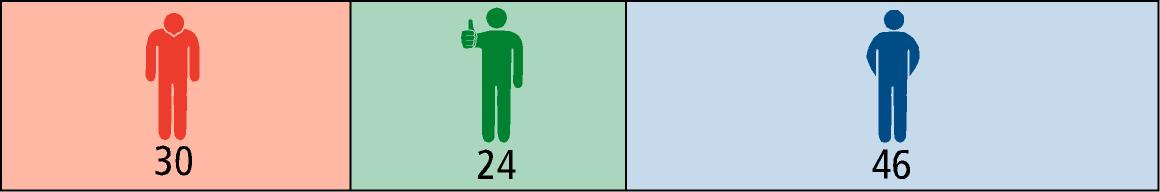 |
|
Natalizumab |
 |
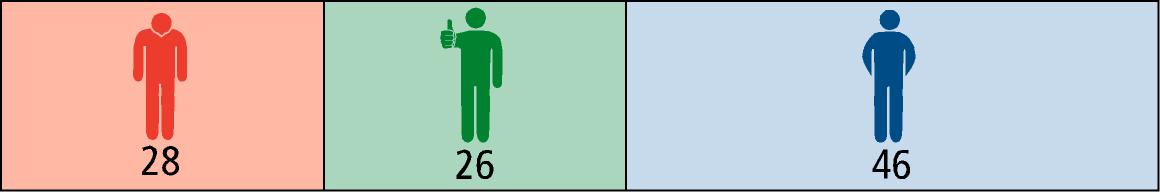 |
| Cladribin (Mavenclad®) |
 |
 |
| Azathioprin (z.B. Imurek®) |
Keine belastbaren Daten zur graphischen Darstellung vorhanden. |  |
| Mitoxantron (z.B. Ralenova®, Novantron®) |
 |
 |
|
Daclizumab (Zinbryta®) |
||
| Im Vergleich zu Rebif® (Beta-Interferon) | ||
| Ocrelizumab (Ocrevus®) |
 |
 |
| Im Vergleich zu Rebif® (Beta-Interferon) | ||
| Alemtuzumab (Lemtrada®) |
Basistherapie | |
 |
 |
|
| Eskalationstherapie | ||
 |
 |
|
| Fußnoten: | *1 Die Ergebnisse der dargestellten Studien sind nicht statistisch signifikant, das heißt der scheinbare Nutzen könnte auf einem Zufall beruhen. Allerdings wurden die hier dargestellten Endpunkte (Zunahme der Behinderung und Schubfreiheit) nicht vordergründig untersucht. Mehr Informationen zu Endpunkten finden Sie hier. | |
