Die Gesamtzahl an Nebenwirkungen wird in den Zulassungsstudien meist nicht berichtet. Je älter die Studien, desto uneinheitlicher die Dokumentation. Deshalb lassen sich die Daten zur schubförmigen MS hier auch nicht zusammenfassen. Zur sekundär chronischen MS lässt sich für 5 Zulassungsstudien mit 3082 Patienten zusammenfassen, dass schwere Nebenwirkungen mit 12% in den Interferon-beta-Gruppen genauso häufig auftraten wie unter Placebo. Therapieabbrüche wegen Nebenwirkungen fanden sich mit 10% signifikant häufiger mit Interferon-beta als mit Placebo (4%). Zur Übersichtlichkeit sind im Folgenden die Nebenwirkungen aus den Zulassungsstudien zur schubförmigen MS zusammengefasst. Diese sind bei den KIS-Studien und bei der sekundär chronischen MS ähnlich. Mögliche Unterschiede werden im Text erwähnt.
Grundsätzlich ist wichtig zu wissen, dass Nebenwirkungen in Studien nicht nur bei den Patienten auftreten, die ein neues Medikament erhalten, sondern auch in der Studiengruppe mit einem bekannten Medikament oder Placebo (siehe "Allgemeines zu Wirkungen und Nebenwirkungen von MS-Medikamenten").
Häufige Nebenwirkungen
In der Tabelle sind Nebenwirkungen aufgeführt, die aus der Cochrane Analyse (Rice 2001[1]) berichtet wurden und bei mindestens 2% der Patienten auftraten. Angegeben ist die Patientenzahl von 100 Patienten.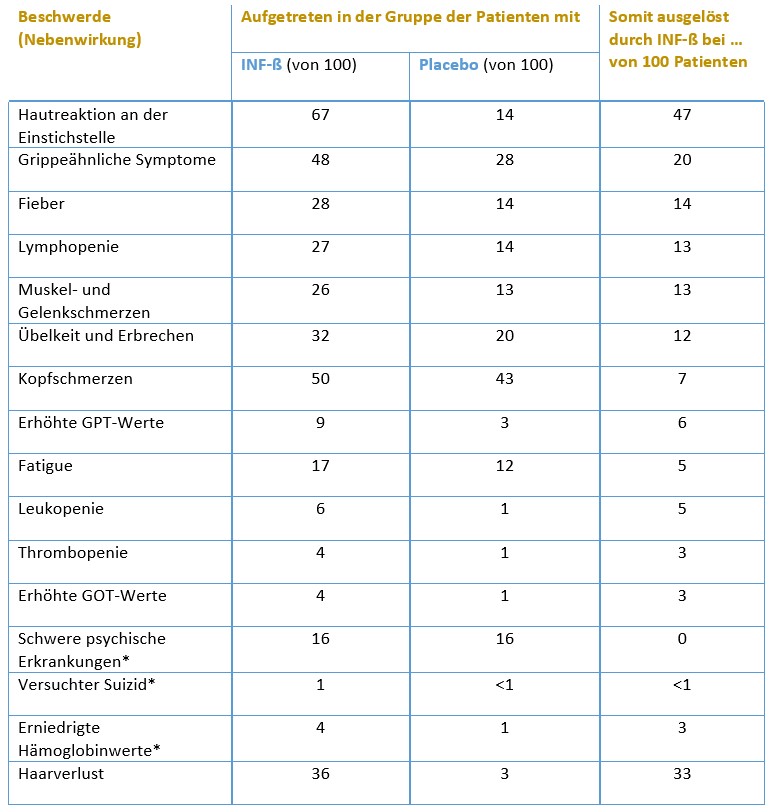
*Bei diesen Nebenwirkungen war der Unterschied zwischen der Interferon-beta- und der Placebo-Gruppe nicht statistisch signifikant.
(Bedingt durch das Runden der Zahlen können kleine Unterschiede (1 von 100) zwischen der Tabelle und der am Kapitelanfang gezeigten Grafik entstehen.)
Reaktionen an der Einstichstelle
Bei der Therapie mit Interferon-beta treten Einstichreaktionen bei subkutaner Gabe mit Betaferon®, Extavia®, Rebif®, Plegridy® sehr häufig auf (zu 50% therapiebedingt). Diese bestehen aus Rötungen und können wochenlang anhalten. Bei intramuskulärerer Gabe werden diese nicht berichtet. Selten kommt es zu schmerzhaften Schwellungen. In manchen Fällen geht das Auftreten von Einstichreaktionen nach und nach zurück. Von offenen Wunden oder auch Nekrosen werden in den Studien bei 2-6% berichtet[100]. Diese heilen wieder ab, bilden dann aber Narben. Durch die Verwendung einer Injektionshilfe kann das Auftreten von Hautreaktionen möglicherweise reduziert werden. Bei langandauernder Interferontherapie können auch ohne Nekrosen Vernarbungen oder Verhärtungen im Unterhautfettgewebe entstehen.
Grippeähnliche Beschwerden (Fieber, Kopfschmerz, Muskelschmerz, Fatigue)
Fast die Hälfte der Patienten (48%), die mit Interferon-beta behandelt wurden, hatte Grippesymptome. Aber auch fast 30% der Placebo-Patienten zeigten solche Symptome. Die Beschwerden setzen meist drei bis acht Stunden nach Medikamentengabe ein und halten bis zu 24 Stunden ein. Dabei können auftreten: Fieber, Schüttelfrost, Muskel- oder Gelenkschmerzen, Kopfschmerzen, Abgeschlagenheit und Müdigkeit.
Die Beschwerden können im Verlauf der Therapie abklingen, dann aber auch irgendwann wieder erneut auftreten. Bei der Betaferon®-Zulassungsstudie hatten nach einem Jahr noch 8%, bei Rebif® je nach Dosierung 5% bzw. 21% diese Nebenwirkungen. Auch wenn grippe-ähnliche Nebenwirkungen im zweiten Therapiejahr seltener berichtetet werden, so finden sich auch nach 16 Jahren mit Betaferon Therapie bei 1/3 noch berichtete grippeähnliche Beschwerden.
Einige Patienten haben den Eindruck, dass sich die Krankheit unter Einnahme des Interferons verschlechtert, denn bedingt durch die Nebenwirkungen können Müdigkeit und Spastiken verstärkt werden. Um grippeähnliche Nebenwirkungen zu vermindern, kann vier Stunden vor und evtl. erneut vier Stunden nach Medikamentengabe ein entzündungshemmendes Schmerzmittel (z.B. Paracetamol oder Ibuprofen) eingenommen werden. Sinnvollerweise wird das Interferon abends vor der Schlafenszeit gespritzt, um die Nebenwirkungen weitgehend unbemerkt „auszuschlafen“. Um die Nebenwirkungen von Beginn an gering zu halten, sollte einschleichend behandelt werden, das heißt, die Therapie sollte mit der halben oder evtl. sogar einem Viertel der Injektionsdosis begonnen werden.
Eine kontrollierte Studie[101] mit 160 Patienten konnte zeigen, dass Paracetamol und Ibuprofen gleichermaßen diese Nebenwirkung lindern. Eine andere Studie[33] verglich den Nutzen von Aspirin, Ibuprofen und einer vierwöchigen niedrigdosierten Kortison-Therapie bei 84 Patienten. Auch wenn insgesamt grippeähnliche Nebenwirkungen bei allen gleich häufig und gleich schwer auftraten, so zeigte die Gruppe mit Ibuprofen-Therapie am Tag der Injektion weniger Beschwerden.
Übelkeit und Erbrechen
Übelkeit und Erbrechen treten etwas häufiger unter Interferon-beta auf[1].
Haarausfall
Verstärkter Haarausfall wurde in 2 kleinen Studien mit insgesamt 82 Patienten bei 15 unter Interferon-beta und nur 1 unter Placebo berichtet.
Leukopenie, Lymphopenie, Thrombopenie
Bei 5 von 100 Patienten entwickelt sich durch die Interferon-Therapie eine Reduktion der Anzahl an weißen Blutzellen (sogenannte Leukopenie). In Einzelfällen können diese weißen Blutzellen unter 3.000/Mikroliter fallen (Normalbereich: 3.800-10.500/μl). Nur selten können Verminderungen der Blutplättchen (eine sogenannte Thrombopenie) auftreten. Bislang sind aber noch keine Fälle bekannt, bei denen diese Veränderungen zu ernsthaften Komplikationen geführt haben.
Leberwerterhöhungen
Leberwerterhöhungen und Interferon-Beta sind häufig. GPT(heute ALT, nur in der Leber vorkommend) und GOT(heute AST, neben Leber auch in Herz, roten Blutzellen und Muskel vorhanden) sind Enzyme des Aminosäurestoffwechsels in der Leber. Bei einer Leberzellschädigung werden sie in das Blut freigesetzt und können labortechnisch festgestellt werden.
In einer Übersichtsarbeit wurden zur Leberwerterhöhung Daten von 2819 Patienten unter Interferon-beta-1A ausgewertet. Innerhalb von zwei Jahren entwickelten 67% der Patienten im Blut nachweisbare Leberwerterhöhungen, ohne jedoch dahingehende Beschwerden zu haben. Bei 15-20% sind diese Werte bis zu 5-fach über dem Normalwert gegenüber 5% der Placebo-Patienten. Die Laborwerte normalisierten sich wieder, zum Teil nach vorübergehender Dosisreduktion. Nur bei 4 von 1.000 Patienten wurde die Therapie aufgrund der Leberwerterhöhungen abgebrochen. Dies Risiko scheint im ersten Jahr der Therapie am höchsten. Das Risiko ist erhöht, wenn zusätzlich viel Alkohol getrunken wird, Patienten fettleibig sind oder andere Medikamente genommen werden, die die Leberfunktion beanspruchen. Empfehlungen von Experten gehen dahin, bei Erhöhungen um mehr als das 20-fache des Normalwerts die Therapie vorübergehend auszusetzen. Bislang wurde nur in Einzelfällen von Leberschädigungen unter Beta-Interferon berichtet.
Schwere Nebenwirkungen und Todesfälle
Durch Interferon-beta bedingte schwere Nebenwirkungen und Todesfälle traten in den Studien nicht gehäuft auf. In einer der KIS-Studien[102] kam es in der Interferon-Gruppe zu einem Toten durch einen Autounfall. In den Studien zur schubförmigen MS kam es unter Betaferon zu einem Selbstmord, in der Rebif-Studie zur schubförmigen MS (PRISMS[6]) kam es zu je einem Todesfall unter Placebo und einem unter 22ug Rebif. Bei den SPMS-Studien traten Todesfälle laut einer Metaanalyse[103] etwas häufiger mit Interferon-beta auf. Unter Interferon-beta kam es zu 17 Todesfällen, 4 durch Selbstmord, 3 Lungenembolien, 3 Herzstillstände, 1 Krebserkrankung, eine Blutung im Kopf, 2 Schlaganfälle und eine schwere Harnwegsinfektion; bei zwei Fällen blieb die Ursache unklar. In den Kontrollgruppen kam es insgesamt zu 7 Todesfällen: 2 Selbstmorde, eine Blutung im Kopf, eine Gefäßerkrankung (Arteriosklerose), eine Lungenentzündung, 2 unbekannte Todesursachen.
In der Fachliteratur sind Einzelfälle schwerer Nebenwirkungen beschrieben, bei denen ein Zusammenhang folgender Beschwerden mit der Interferon-Gabe für wahrscheinlich gehalten wird: Blutarmut, Überaktivität der Schilddrüse, Nierenfunktionsausfall, Verstopfung von kleinen Blutgefäßen, allergischer Schock und epileptische Anfälle. Weiter finden sich vereinzelt Entzündungen im Fettgewebe der Haut und andere Hautveränderungen sowie Leberentzündungen und Muskelschädigungen.
Krebserkrankungen
In den Studien wird nur bei der SPMS eine Krebserkrankung aus einer Interferon-beta-Gruppe beschrieben. Oft fehlt in den Studien jede Aussage zu möglichen Krebserkrankungen. Damit ist eine belastbare Risikoeinschätzung nicht möglich. Es erscheint aber heute, 25 Jahre nach Zulassung der ersten Interferone, mit keinerlei Langzeithinweis auf Krebserkrankungen sehr unwahrscheinlich, dass Interferone Krebserkrankungen hervorrufen.
Infektionen
Infekte traten bei der Therapie mit Interferonen nicht gehäuft auf. Auch die Langzeitstudien sprechen nicht dafür.
Welche neuen Nebenwirkungen wurden nach Abschluss der Zulassungsstudien berichtet?
Einzelfälle von akutem Leberversagen sowie von einer akuten Nierenerkrankung mit Eiweißverlust sind im Verlauf nach Zulassung der Interferon-beta-Präparate beschrieben worden. Weitere besondere Nebenwirkungen sind 25 Jahre nach der ersten Interferon-Zulassung nicht berichtet worden.
