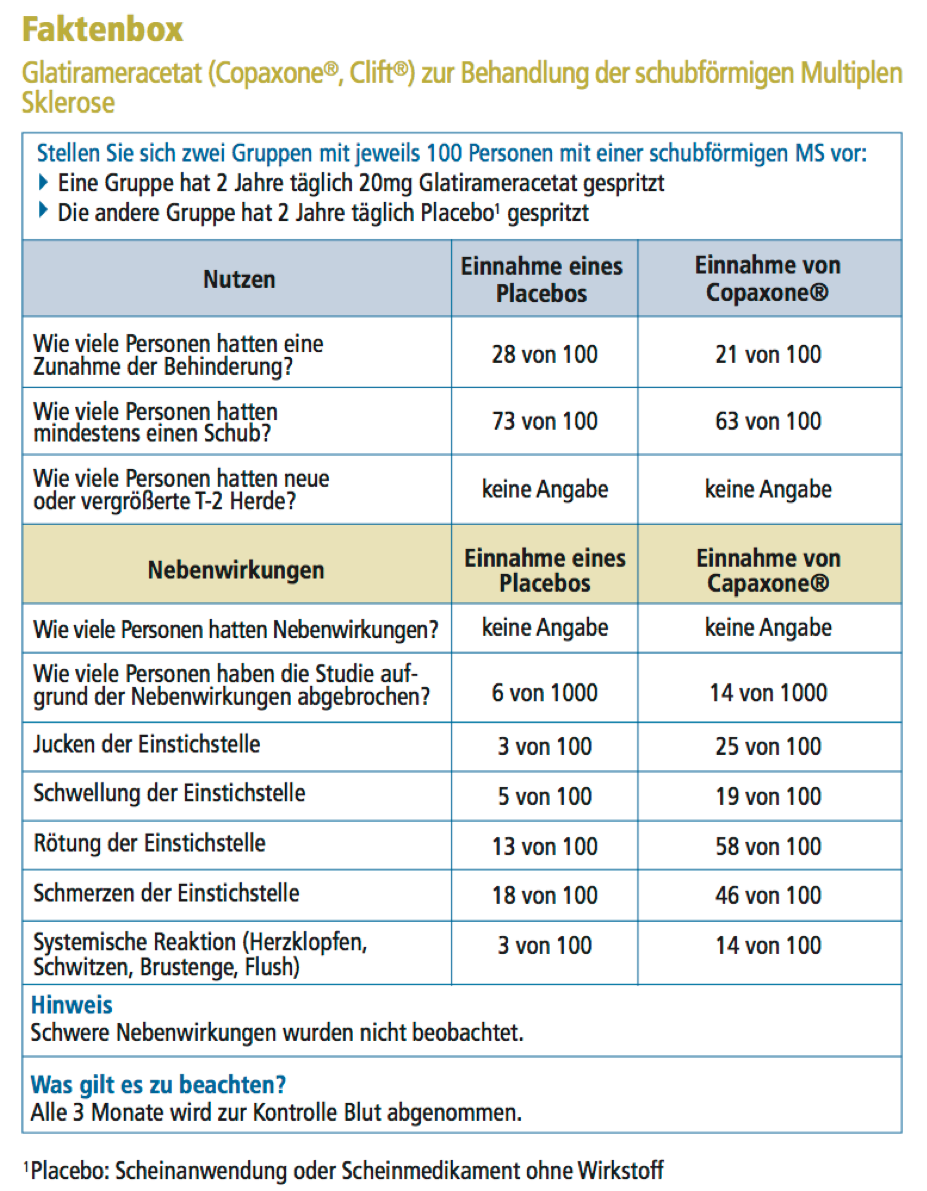
Glatirameracetat (Copaxone®, Clift®)
Glatirameracetat ist in Deutschland seit 2001 zugelassen. Es wird als Injektion zwischen einmal täglich und dreimal pro Woche ins Unterhautfettgewebe gespritzt. Bei einem Teil der Patienten reduziert Glatirameracetat die Schubrate und hält die Zunahme der Behinderung auf. An wichtigen Nebenwirkungen treten häufig eine Einstichreaktion und eine systemische Reaktion (Herzrasen, Schwitzen, Brustschmerz, Flush), die maximal 30 Minuten anhält, auf. Das Medikament wird in der Apotheke unter dem Namen Copaxone® vertrieben, ein Nachahmerpräparat gibt es unter dem Namen Clift®.
Wirkungen & Nebenwirkungen im grafischen Überblick
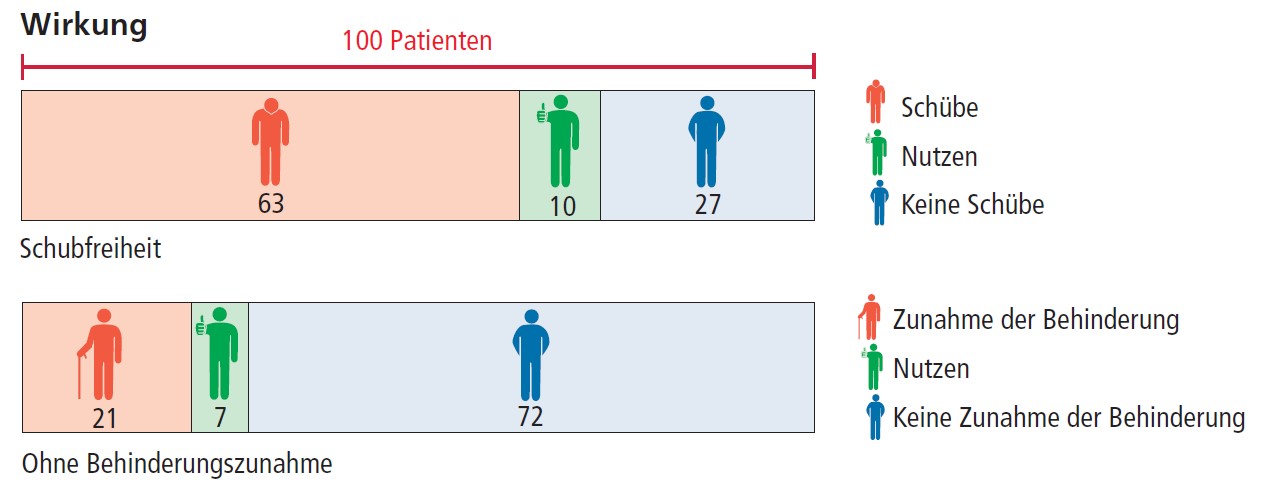
Eine detaillierte Erklärung finden Sie in den Kapiteln Schubfreie Patienten und Patienten ohne Zunahme der Behinderung .
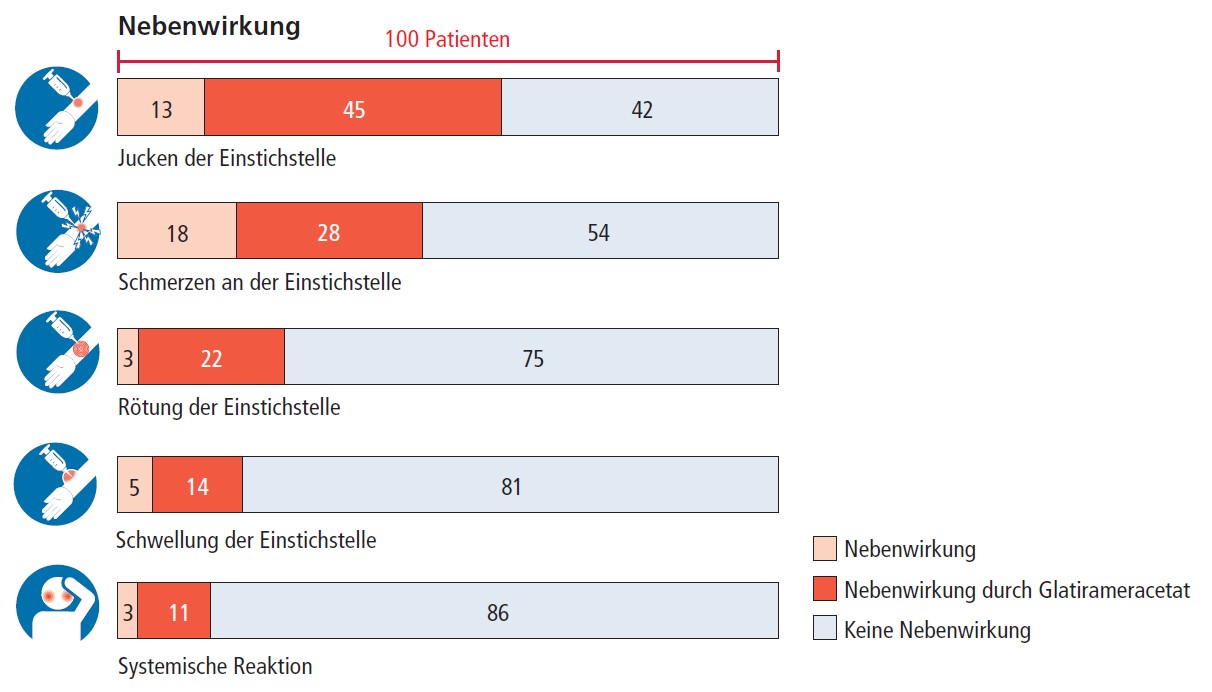
In dem Kapitel Nebenwirkungen finden Sie eine detaillierte Erklärung zu den Nebenwirkungen des Medikaments.
Was ist Glatirameracetat?
Glatirameracetat ist ein künstlich hergestelltes Eiweißgemisch. In seinem Aufbau ähnelt es stark den Bausteinen der Isolierschicht im zentralen Nervensystem, dem sogenannten Myelin.
Erstmals wurde Glatirameracetat in den 60-er Jahren hergestellt. Es besteht aus vier Eiweißstoffen, sogenannten Aminosäuren, aus denen sich auch der Name des Medikaments zusammensetzt: Glutamin, Lysin, Alanin und Tyrosin.
Bei den Untersuchungen mit Copaxone® stellte sich heraus, dass es vor MS schützt. In den Folgejahren war die industrielle Herstellung großer Mengen von Copaxone® für Studien ein Hauptproblem: Zwar kann man das Mengenverhältnis der Eiweißbaustoffe bei der Herstellung des Medikaments festlegen, aber der Prozess der Verknüpfung der Aminosäuren zu langen Ketten (sogenannte Polymere) lässt sich nur begrenzt steuern. Deshalb muss auch jede neu produzierte Menge des Medikaments im Tierversuch erneut auf seine Wirksamkeit überprüft werden.
Wie wirkt Glatirameracetat?
Zur Wirkungsweise von Glatirameracetat bestehen nur Modellvorstellungen, da der genaue Wirkmechanismus noch nicht komplett verstanden ist. Vermutet wird, dass Glatirameracetat wie eine Art Desensibilisierung wirkt, die man auch zur Behandlung von Allergien nutzt. Durch die Konfrontation mit einer dem Myelin ähnlichen Substanz soll das Immunsystem wieder lernen, Myelin zu tolerieren und nicht anzugreifen.
Für wen ist Glatirameracetat zugelassen?
Glatirameracetat 20mg/ml (Copaxone®) ist in Europa seit 2001 zur Behandlung von Erwachsenen mit schubförmig verlaufender Multipler Sklerose zugelassen. Seit 2015 ist Copaxone® auch mit 40mg/ml Konzentration zugelassen. Unter dem Namen Clift® wurde in Europa 2016 ein Nachahmerpräparat von Copaxone® in 20mg/ml Konzentration zugelassen, 2017 folgte Clift® in 40mg/ml Konzentration.
Wie wird Glatirameracetat verabreicht?
Glatirameracetat existiert als fertige Einmalspritzen in 20mg- oder 40mg-Konzentration. Es wird mithilfe dieser Fertigspritzen ins Unterhautfettgewebe gespritzt, also subkutan. Die Fertigspritzen gibt es als 20mg/ml (Einnahme täglich) und 40mg/ml (Einnahme dreimal wöchentlich) Konzentration. Folglich werden entweder 20mg täglich ins Unterhautfettgewebe gespritzt oder 40mg dreimal pro Woche. Ob man die tägliche, niedriger dosierte Spritze oder die dreimal wöchentliche, höher dosierte Spritze verwendet, hat keinen Einfluss auf den Therapieerfolg und kann nach persönlichem Belieben gemeinsam mit dem Arzt entschieden werden.
Die Einleitung der Therapie sollte von einem Neurologen überwacht werden.
Auf dem Foto sehen Sie beispielhaft eine Medikamentenpackung sowie eine Einmalspritze von Copaxone®.

Bildquelle: https://www.apotheke-adhoc.de/nachrichten/detail/pharmazie/copaxone-als-pen-ohne-ausloeseknopf-aber-mit-neuem-logo-multiple-sklerose/
Wie wirksam ist Glatirameracetat bei schubförmiger MS?
Im Glossar finden Sie unter „Allgemeines zu Wirkungen und Nebenwirkungen von MS-Medikamenten“ eine allgemeine Einführung in die Thematik, welche Ihnen helfen kann, die nachfolgenden Informationen zur Wirkung von Glatirameracetat besser zu verstehen.
Die folgenden Daten beziehen sich zunächst auf die 20-mg-Konzentration; Informationen zur 40-mg-Dosis finden Sie weiter unten im Kapitel.
Wirkung beim klinisch isolierten Syndrom (KIS)
Copaxone® ist seit 2009 in Deutschland auch für Patienten mit KIS zugelassen. Als KIS (englisch: clinically isolated syndrome, kurz CIS) bezeichnet man die ersten Beschwerden, die auf eine MS hindeuten, also einen ersten Schub. Zusatzuntersuchungen liegen in diesem Krankheitsstadium noch nicht vor oder die Ergebnisse lassen noch keine sichere MS-Diagnose zu.
In der PRECISE Studie[92] von Comi et al. 2009 wurden 481 Patienten mit KIS aufgeteilt in zwei Gruppen: Eine Gruppe erhielt täglich eine Placebo-Injektion, die andere eine tägliche Injektion mit 20mg/ml Copaxone®. Patienten, die einen zweiten Schub hatten, wurden aus der Studie entfernt und nahmen nicht in den ganzen 3 Jahren teil. Die teilnehmenden Patienten mussten für die Studie eine unifokale Manifestation und mindestens 2 T2-Läsionen im MRT haben. Endpunkte der Studie waren dabei der Übergang zu klinisch diagnositzierter MS durch einen zweiten Schub, die Zeit bis zu einem zweiten Schub und beobachtete Nebenwirkungen.
Es ergab sich, dass in den beobachteteten drei Jahren 18 von 100 Patienten durch Copaxone zusätzlich ohne 2. Schub blieben: 43 von 100 in der Placebogruppe und 25 von 100 in der Glatirameracetat-Gruppe hatten einen zweiten Schub. 45 con 100 Patienten blieben durch Glatirameracetat zusätzlich ohne zweiten Schub. Außerdem ergab sich eine Verlängerung der Zeit bis zum zweiten Schub von durchschnittlich 336 Tagen bei Placebo-Einnahme zu 772 Tagen bei Copaxone®-Einnahme. Die beobachteten Nebenwirkungen waren die Injektionsreaktion und die systemische Reaktion, die auch in anderen Studien beobachtet wurden (siehe weiter unten im Kapitel „Welche Nebenwirkungen hat Glatirameracetat?“).
1. Wirkung auf die Schubfreiheit bei schubförmiger MS
Die Grafik am Kapitelanfang zeigt, wie viele Patienten nach 2 Jahren Therapie mit Glatirameracetat oder Einnahme von Placebos noch schubfrei waren. Daraus kann man den absoluten Nutzen (absolute Risikoreduktion) und den relativen Nutzen (relative Risikoreduktion) berechnen.
Hier wird die Anzahl der Patienten mit Schüben beschrieben. Um Studienergebnisse mit unterschiedlichen Teilnehmerzahlen besser vergleichen zu können, werden die Ergebnisse bezogen auf 100 Patienten dargestellt:
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl von Patienten mit Schüben in der Glatirameracetat-Gruppe (63) von denen mit Schüben in der Placebo-Gruppe (73) abzieht. Tatsächlich profitieren 73 – 63, also 10 von 100 Patienten von der Therapie. Das entspricht dem absoluten Nutzen (oder auch der absoluten Risikoreduktion).
- 10 von 100 Patienten haben einen Nutzen von der Therapie.
- 63 von 100 Patienten profitieren nicht von der Therapie, da sie trotz der Einnahme von Glatirameracetat einen Schub hatten.
- 27 von 100 Patienten profitieren nicht, da sie auch ohne Glatirameracetat schubfrei geblieben sind.
2. Wirkung auf die Anzahl der Schübe pro Jahr bei schubförmiger MS
Die jährliche Schubrate zeigt, wie viele Schübe durchschnittlich pro Jahr pro Patient auftraten. Daten für die jährliche Schubrate werden nicht in allen Studien berichtet, in einer der Zulassungsstudien beträgt sie in der Placebo-Gruppe 0,84 Schübe gegenüber 0,59 Schüben in der Glatirameracetat-Gruppe. Etwas verständlicher ausgedrückt: Die Patienten in der Placebo-Gruppe haben im Durchschnitt alle 14 Monate einen Schub, die Patienten in der Glatirameracetat-Gruppe nur alle 20 Monate.
3. Wirkung auf die Zunahme der Behinderung bei schubförmiger MS
Die Zunahme der Behinderung wurde in den oben beschriebenen Zulassungsstudien mithilfe des EDSS gemessen, einer Behinderungsskala von 0 bis 10 (wobei 0 keiner Behinderung entspricht). Die Grafik am Kapitelanfang zeigt, wie viele Patienten nach einer zweijährigen Therapie mit Glatirameracetat bzw. zweijähriger Einnahme von Placebos keine Zunahme der Behinderung hatten. Dargestellt sind wieder der absolute Nutzen (absolute Risikoreduktion) und der relative Nutzen.
Im Glossar finden Sie Angaben zum Nutzen von Medikamenten bei anderen Erkrankungen. So bekommen Sie einen Eindruck davon, wie groß die Therapieeffekte bei MS im Vergleich zu denen bei anderen Krankheiten sind.
Im Folgenden wird die Entwicklung der Behinderung in zwei Jahren beschrieben, jeweils bezogen auf 100 Patienten:
- 21 von 100 Patienten haben trotz der Glatirameracetat-Therapie eine Zunahme der Behinderung
- 72 von 100 Patienten profitieren nicht von der Therapie, sie haben unabhängig von der Therapie keine Zunahme der Behinderung
- 7 von 100 Patienten haben durch die Einnahme von Glatirameracetat keine Zunahme der Behinderung
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl von Patienten mit einer Behinderungszunahme in der Glatirameracetat-Gruppe (21) von denen mit einer Behinderungszunahme in der Placebo-Gruppe (28) abzieht. Hier profitieren 28 – 21, also 7 von 100 Patienten von der Therapie.
Glatirameracetat in 40mg/ml Konzentration
Glatirameracetat ist in der 40mg/ml Konzentration mit Injektion alle 2 Tage seit 2015 auch in Europa zugelassen, nachdem in einer Studie[89] (siehe weiter oben im Kapitel „Welche Zulassungsstudien wurden für Glatirameracetat durchgeführt?“) 1534 Patienten entweder Placebo oder 40mg Glatirameracetat über 12 Monate einnahmen. Das Ergebnis zeigte, dass mit Glatirameracetat 40mg/ml 34 von 100 Patienten zusätzlich im Vergleich zu Placebo zusätzlich schubfrei blieben. Auch hatten zusätzliche 35 von 100 Patienten weniger neue oder vergrößerte T2-Läsionen im MRT. An Nebenwirkungen traten am häufigsten die Injektionsreaktionen auf, die auch bei Glatirameracetat 20mg/ml beobachtet wurden.
4. Wirkung auf die MRT/das Kernspin in zwei Jahren bei schubförmiger MS
Die Wirkung von Glatirameracetat auf MRT-Bilder wurde in Studien nur über 9 Monate getestet (Comi 2001[40]) und ist deshalb nur begrenzt interpretierbar. In der Studie wurden 239 Personen mit schubförmiger MS über 9 Monate entweder 20mg Glatirameracetat oder Placebo täglich gespritzt, mit dem Ergebnis, dass Glatirameracetat signifikant die Krankheitsaktivität im MRT senkt.
Im Glossar finden Sie Daten zu dem Anteil der Patienten, bei denen es über 2 Jahre keine Anzeichen einer Krankheitsaktivität gab (NEDA - no evidence of disease activity).
Zulassungsstudien
Die Wirkung von Glatirameracetat in der 20-mg-Dosis auf die Schubrate und die Zunahme der Behinderung wurde in mehreren Zulassungsstudien (Bornstein 1987[38]) und Johnson 1995[39]) geprüft und veröffentlicht. Insgesamt wurden in den beiden Studien 301 Patienten mit schubförmiger Multiple Sklerose über einen Zeitraum von 2 Jahren untersucht. Eingeschlossen wurden Patienten, die in den 2 Jahren vor Studienbeginn mindestens 2 dokumentierte Schübe hatten und einen EDSS-Score von <6.
In der Vorstudie zur Therapie mit Glatirameracetat von Bornstein et al. 1987 wurden 20mg Glatirameracetat und ein Placebo verglichen. Die Wirkstoffe wurden dabei zufällig verteilt und weder die 51 Patienten noch die Ärzte wussten, welche Substanz die jeweiligen Patienten erhielten.
1995 folgte eine größere Studie von Johnson et. al., in der 250 Patienten zufällig verteilt entweder Placebo oder 20mg Glatirameracetat bekamen. Studienendpunkte waren die Schubfreiheit und die Zunahme von Beeinträchtigung.
Die Zulassung von Copaxone® 40mg beruht vor allem auf Daten aus der randomisiert-kontrollierten GALA-Studie[89] (Phase-III-Glatirameracetat Low-Frequency Administration). Die Daten in den folgenden Kapiteln werden sich allerdings primär auf die niedrigere Dosis beziehen, also Copaxone in 20mg-Konzentration.
Schließlich wurde im Jahr 2000 eine Studie[40] durchgeführt, die ihr Hauptaugenmerk auf mögliche in der Kernspintomografie nachweisbare Wirkungen von Copaxone® richtete. Da diese Studie nur über neun Monate lief, werden die Daten in der folgenden Übersicht nicht berücksichtigt. Die unten aufgeführten Ergebnisse beruhen somit auf Daten von insgesamt 299 behandelten Patienten. Diese wurden kürzlich auch in einem Cochrane Review analysiert. Hauptendpunkt der Studien war die jährliche Schubrate.
Welche Nebenwirkungen hat Glatirameracetat?
Grundsätzlich ist wichtig zu wissen, dass Nebenwirkungen in Studien nicht nur bei den Patienten auftreten, die ein neues Medikament erhalten, sondern auch in der Studiengruppe mit einem bekannten Medikament oder Placebo (siehe „Allgemeines zu Wirkungen und Nebenwirkungen von MS-Medikamenten“).
Häufige Nebenwirkungen
In der Tabelle sind Nebenwirkungen aufgeführt, die aus den beiden Zulassungsstudien berichtet wurden und bei mindestens 2% der Patienten auftraten. Angegeben ist die Patientenzahl von 100 Patienten.
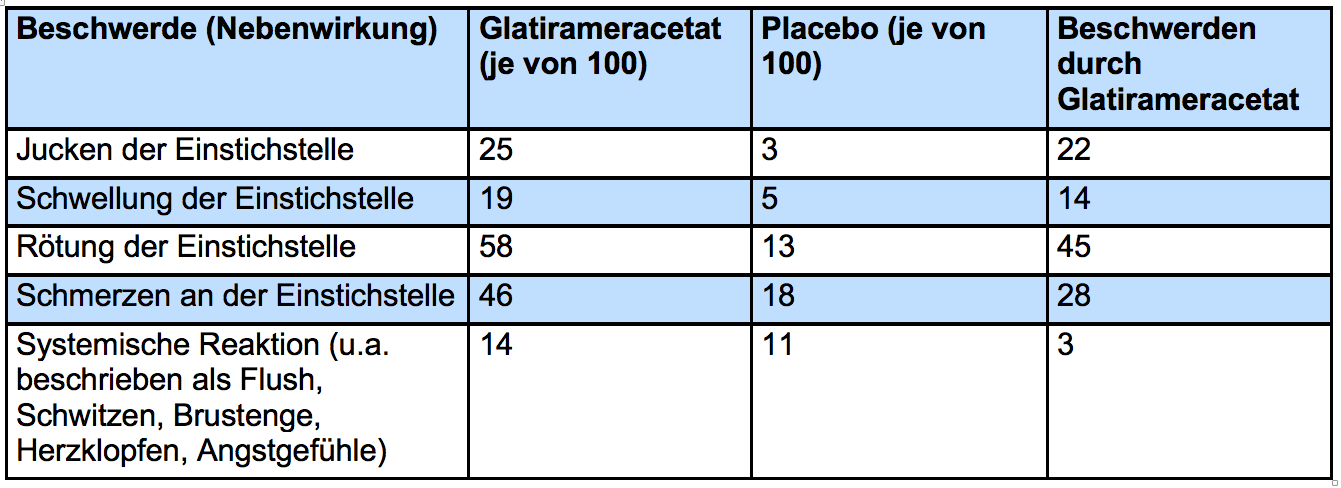
Das sogenannte systemisch inflammatorische Response Syndrom (SIRS) ist eine Kombination aus verschiedenen Beschwerden, wie Gesichtsrötung, Brustenge, Schwitzen, Herzklopfen, Luftnot und Angstgefühle, die einer allergischen Reaktion ähneln. Es ist selbstlimitierend, das heißt, es tritt wenige Minuten nach der Injektion auf und klingt innerhalb von 30 Minuten wieder ab. Komplikationslos. SIRS sind in den Zulassungsstudien bei einzelnen Patienten bis zu 7-mal aufgetreten.
Schwere Nebenwirkungen und Todesfälle
Durch Glatirameracetat bedingte schwere Nebenwirkungen und Todesfälle traten in den Studien nicht gehäuft auf.
Krebserkrankungen
In der Glatirameracetat-Gruppe traten 0 Krebserkrankungen auf und in der Placebo-Gruppe auch 0, d.h. Krebserkrankungen traten bei Glatirameracetat-Einnahme nicht gehäuft auf.
Infektionen
Infekte traten bei der Therapie mit Glatirameracetat nicht gehäuft auf. Dennoch ist zu beachten, dass alle Medikamente, die das Immunsystem beeinflussen, das Infektionsrisiko erhöhen können. Auch dies kann nur in Langzeitstudien geklärt werden.
Welche neuen Nebenwirkungen wurden nach Abschluss der Zulassungsstudien berichtet?
Neue Nebenwirkungen sind seit der Zulassung nicht bekannt geworden.
Worauf muss bei der Therapie mit Glatirameracetat geachtet werden?
Unter welchen Umständen sollte Glatirameracetat nicht eingenommen werden bzw. welche Sicherheitsabstände müssen eingehalten werden?
Glatirameracetat sollte nicht eingenommen werden:
- Bei (vorheriger) Einnahme anderer MS Medikamente:
- Sicherheitsabstand von 4 Wochen bei Einnahme von Teriflunomid (Aubagio®) oder Fingolimod (Gilenya®)
- Sicherheitsabstand von 6-8 Wochen bei Einnahme von Natalizumab (Tysabri®)
- Sicherheitsabstand von 3 Monaten bei Einnahme von Mitoxantron
- Sicherheitsabstand von 6-12 Monaten bei Einnahme von Alemtuzumab (Lemtrada®) oder anderen Antikörpern, die zielgerichtet Immunzellen zerstören
- Bei Einnahme anderer Medikamente, die das Immunsystem beeinträchtigen können
Worauf ist bei Therapiebeginn zu achten?
Weil Glatirameracetat das Immunsystem nicht generell hemmt, sondern nur bestimmte Immunreaktionen, müssen keine besonderen Schutzmaßnahmen wie bspw. Impfungen erfolgen.
Bei Patienten, die bereits eine Therapie erhalten haben, die das Immunsystem beeinflusst oder hemmt, müssen Sicherheitsabstände eingehalten werden (siehe vorangehender Absatz). Diese richten sich nach der Wirkdauer der Medikamente. Eine Kurzzeitbehandlung mit Kortikosteroiden (Kortison), z.B. zur Schubtherapie, ist auch während der Behandlung möglich.
Was muss während der Therapie kontrolliert werden?
Das Krankheitsbezogene Kompetenznetz Multiple Sklerose (KKNMS) empfiehlt:
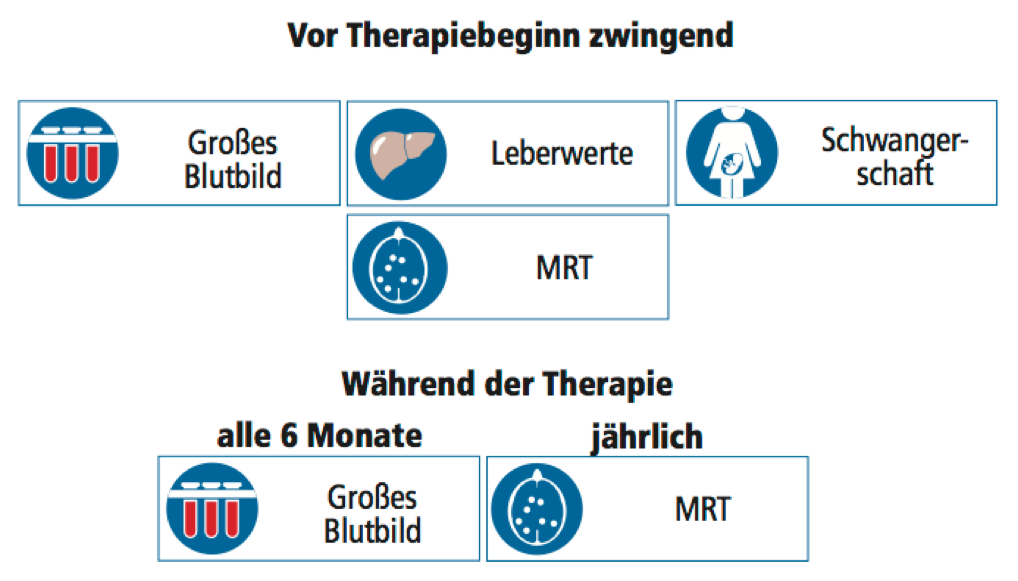
Da Glatirameracetat auf das Immunsystem wirkt, sollten alle 3 Monate Blutuntersuchungen erfolgen. Alle 3 Monate sollte außerdem eine neurologische Untersuchung durchgeführt werden, um die Krankheitsentwicklung und den Therapieerfolg zu beobachten.
Glatirameracetat - Häufig gestellte Fragen
Wirkt Glatirameracetat besser oder schlechter als andere MS-Medikamente?
Es gibt Studien, in denen Glatirameracetat direkt mit Interferon-Beta-Präparaten verglichen wurde. Ein Cochrane Review von La Mantia et. al. (2016) fasst verschiedene Studienergebnisse zusammen. Die Autoren stellen fest, dass die zwei Medikamente einen ähnlichen Effekt auf die Schubrate und die Behinderungsentwicklung haben.
Wie lange wird behandelt?
Glatirameracetat wird als Dauertherapie eingesetzt.
Nutzen und Risiko der Einnahme müssen laufend überprüft werden. Ein Abschätzen des Nutzens ist oft frühestens nach einem Jahr möglich. Als Hinweise für eine Wirksamkeit werden allgemeine Schubfreiheit und das Fehlen neuer Herde im MRT angesehen. Deshalb empfiehlt das KKNMS ein Ausgangs-MRT und ein MRT nach 6, 12 und 24 Monaten, um Nutzen und auch mögliche Risiken abzuschätzen.
Schwangerschaft und Stillzeit
Glatirameracetat kann vermutlich in der Schwangerschaft eingenommen werden. In Tierstudien wurden keine schädlichen Konsequenzen für die Nachkommen beobachtet. Die bisherigen Daten mit 20mg/ml Einnahme täglich von Glatirameracetat bei schwangeren Frauen deuten nicht auf einen Schaden für das Kind hin. Bislang liegen aber keine systematischen, große Studien vor. In den USA und UK wird GA auch in der Schwangerschaft verschrieben. Nach 20 Jahren Sammlung von Daten von über 7000 Frauen, die unter GA schwanger wurden, konnte keine erhöhten Risiken für Kind oder Mutter beobachten konnte. Eine Zulassung für GA während der Schwangerschaft in der EU ist beantragt. In Deutschland gilt aber weiterhin, dass aus Vorsichtsgründen eine Anwendung von GA während der Schwangerschaft vermieden werden sollte, es sei denn, dass der Nutzen für die Mutter das Risiko für den Fetus überwiegt.
Es ist möglich, dass GA in die Muttermilch übergeht, die Einnahme sollte also wenn möglich während der Stillzeit vermieden werden.
Impfungen
Bisher sind keine negativen Effekte auf Impferfolge bekannt. Einige wenige Daten sprechen dafür, dass Standardimpfungen unter Glatirameracetat wirksam bleiben. Empfohlen wird auch unter Glatirameracetat eine (jährliche) Grippeschutzimpfung.
Infektionen
Grundsätzlich muss Glatirameracetat beim Auftreten üblicher Infekte nicht abgesetzt werden. Bei schweren Infekten oder gehäuften Infekten, muss im Einzelfall jedoch ein Absetzen erwogen werden.
Welche Alternativen bestehen zu Glatirameracetat?
Glatirameracetat ist nur eine von verschiedenen zugelassenen MS-Therapien. Eine Übersicht finden Sie zu Anfang des Kapitels. Eine weitere Möglichkeit ist auch, (noch) keine Immuntherapie durchzuführen. Weitere Informationen dazu finden Sie in Kapitel 6 „Was erwartet mich bei Multipler Sklerose ohne Therapie?“.
Ohne Therapie folgt die MS dem natürlichen Verlauf. Wie dieser aussieht, kann man aus den Daten der Placebo-Gruppe in den Zulassungsstudien abschätzen: Über 2 Jahre blieben in der Placebo Gruppe 27 von 100 Patienten schubfrei und 72 von 100 ohne Zunahme der Behinderung.
Glatirameracetat - Alles auf einen Blick