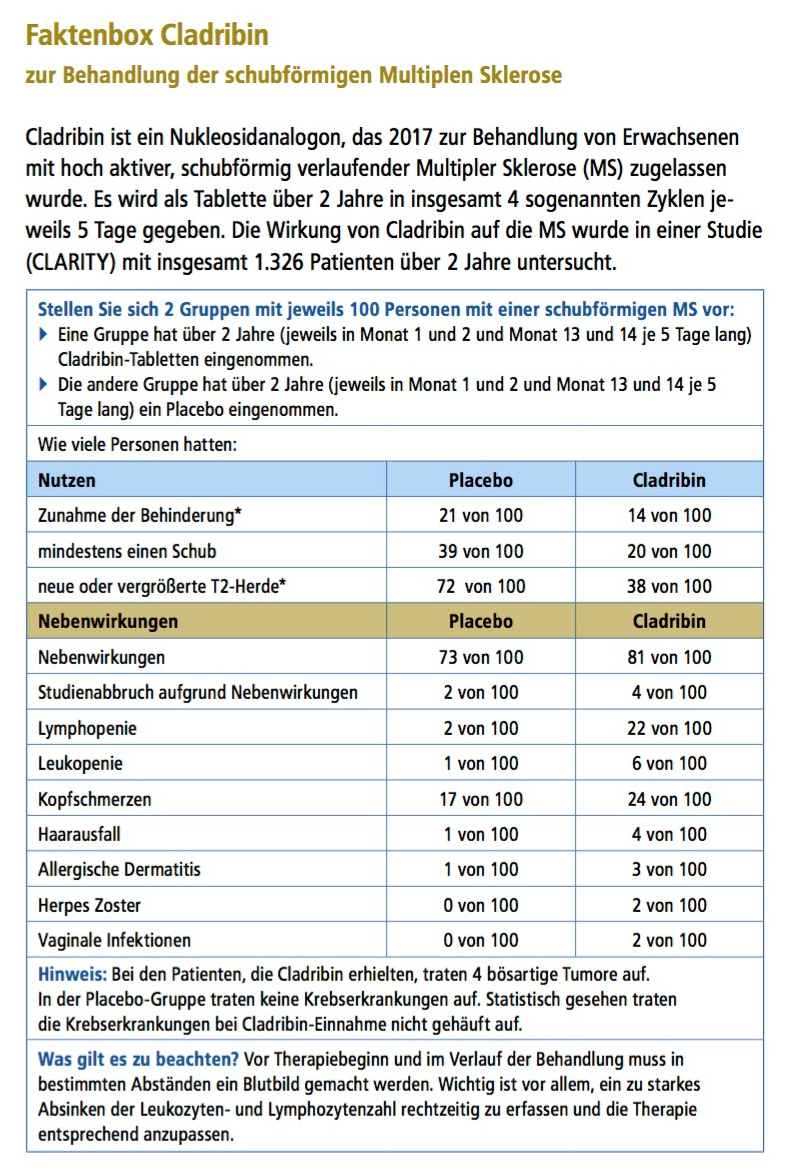
Cladribin (Mavenclad®)
Cladribin (Mavenclad®) wird als Tablette über zwei Jahre in vier Zyklen von jeweils fünf Tagen eingenommen. Es ist zugelassen für Patienten mit hochaktiver schubförmiger Multipler Sklerose. Bei einem Teil der Patienten reduziert es die Häufigkeit von Schüben und hält die Zunahme der Behinderung auf. Dass Cladribin so selten eingenommen werden muss, liegt daran, dass das Medikament das Immunsystem sehr langfristig beeinflusst.
Nebenwirkungen, die bei der Einnahme von Cladribin in Studien auftraten, waren Kopfschmerzen und eine Verminderung der weißen Blutzellen (Leukozyten). Diese Verminderung betrifft vor allem eine Untergruppe der Leukozyten, die Lymphozyten. Die Anzahl der weißen Blutzellen muss deshalb mithilfe einer Blutuntersuchung in regelmäßigen Abständen bestimmt werden („großes Blutbild“). Wenn die Zahl der Lymphozyten unter einen bestimmten Grenzwert fällt, sollte keine Medikamentengabe erfolgen, bis sich die Werte wieder normalisiert haben.
Wirkungen und Nebenwirkungen im Überblick
Was ist Cladribin?
Cladribin (auch „2-Chlorodesoxyadenosin“) gehört zur Gruppe der sogenannten Nukleosidanaloga. Nukleoside sind Bausteine der DNS; dementsprechend sind Nukleosidanaloga Moleküle, die den Bausteinen des menschlichen Erbguts sehr ähnlich sind. Wenn Zellen diese fremden Bausteine in ihr Erbgut einbauen, wird ihre Funktion gestört und sie gehen schneller zugrunde als üblich. Cladribin kann deshalb auch Krebszellen bekämpfen und ist seit einigen Jahren als Chemotherapie bei einer Blutzellkrebserkrankung, der Haarzellleukämie, zugelassen.
Wie wirkt Cladribin?
Cladribin gehört zu den sogenannten Immuntherapien der MS. Das Immuntherapeutikum wirkt besonders auf bestimmte Untergruppen von weißen Blutkörperchen (die Lymphozyten), von denen es bevorzugt aufgenommen wird. Weil Cladribin den Bausteinen der DNS so ähnlich sieht, wird es von den Zellen fälschlicherweise in deren Erbgut eingebaut. Das bewirkt, dass die Lymphozyten nicht mehr richtig funktionieren und sich auch nicht mehr teilen können.
Auf diese Weise wird die Anzahl der Lymphozyten vorübergehend reduziert und bestimmte Funktionen werden gestört.
Für wen ist Cladribin zugelassen?
Cladribin ist in der EU seit August 2017 für Patienten mit hochaktiver schubförmiger Multipler Sklerose zugelassen. „Hochaktiv“ wurde in der Studie, die zur Zulassung führte, definiert als:
- Patienten, die im vorausgegangenen Jahr einen Schub und in der MRT mindestens eine Kontrastmittel aufnehmende Läsion, alternativ neun oder mehr T2-Läsionen während der Behandlung mit anderen Immuntherapien hatten,
- Patienten mit zwei oder mehr Schüben im vorausgegangenen Jahr, unabhängig davon, ob sie mit einer Immuntherapie behandelt wurden oder nicht.
Wie wird Cladribin eingenommen?
Cladribin ist als Tablette erhältlich. Es wird nicht wie andere Tabletten täglich, sondern in insgesamt vier Behandlungszyklen über zwei Jahre eingenommen, sprich zwei Behandlungszyklen pro Jahr. In beiden Jahren gibt es je zwei Behandlungszyklen von 4 – 5 Tagen im Abstand von einem Monat.
Konkret heißt das, dass Patienten jeweils in Monat 1 und 2 sowie Monat 13 und 14 der Behandlung 4 bis 5 Tage lang Cladribin-Tabletten erhalten. Die Dosis, also wie viele Tabletten ein Patient genau einnehmen muss, richtet sich nach seinem Körpergewicht. Pro Kilogramm Körpergewicht müssen über zwei Jahre insgesamt 3,5 mg Cladribin eingenommen werden. Das nennt sich „kumulative Dosis“. Die kumulative Dosis wird wegen der vier Zyklen durch 4 geteilt. Das Ergebnis wird auf vier bis fünf Tage verteilt.
Beispielsweise sieht die Rechnung für einen 60 Kilogramm (kg) schweren Patienten folgendermaßen aus:
Kumulative Dosis: 60kg x 3,5mg Wirkstoff = 210mg
Dosis pro Behandlung: 210mg/4 Zyklen = 52,5mg/Zyklus
Dosis pro Tag (in 10-mg-Tabletten): 52,5mg/5 Tage = 1 x 10mg/Tag
Das heißt, ein 60kg schwerer Patient würde in Monat 1 und 2 sowie in Monat 13 und 14 für 5 Tage je eine 10-mg-Tablette Cladribin einnehmen.
Wird die Einnahme einer Tablette vergessen, so darf sie nicht am darauffolgenden Tag zusammen mit der nächsten Tablette eingenommen werden, sondern der Zeitraum der Einnahme verlängert sich dementsprechend um einen Tag.
Die Tabletten können unabhängig von den Mahlzeiten eingenommen werden. Sie müssen mit Wasser eingenommen und unzerkaut heruntergeschluckt werden. Weil sie keinen Filmüberzug haben, müssen sie nach der Entnahme aus der Packung sofort eingenommen werden. Bei der gleichzeitigen Einnahme anderer oraler Arzneimittel empfiehlt die Europäische Arzneimittel-Agentur (EMA), an den wenigen Tagen, an denen Cladribin eingenommen wird, einen zeitlichen Abstand von drei Stunden zur Einnahme anderer Medikamente einzuhalten.
Links sehen Sie ein Foto der Medikamentenpackung von Mavenclad® und rechts ein Foto der Tabletten: 
Bildquelle: https://www.deutsche-apotheker-zeitung.de/news/artikel/2019/04/01/cladribin-bei-sekundaer-progredienter-ms
Wie wirksam ist Cladribin bei schubförmiger MS?
1. Wirkung auf die Schubfreiheit
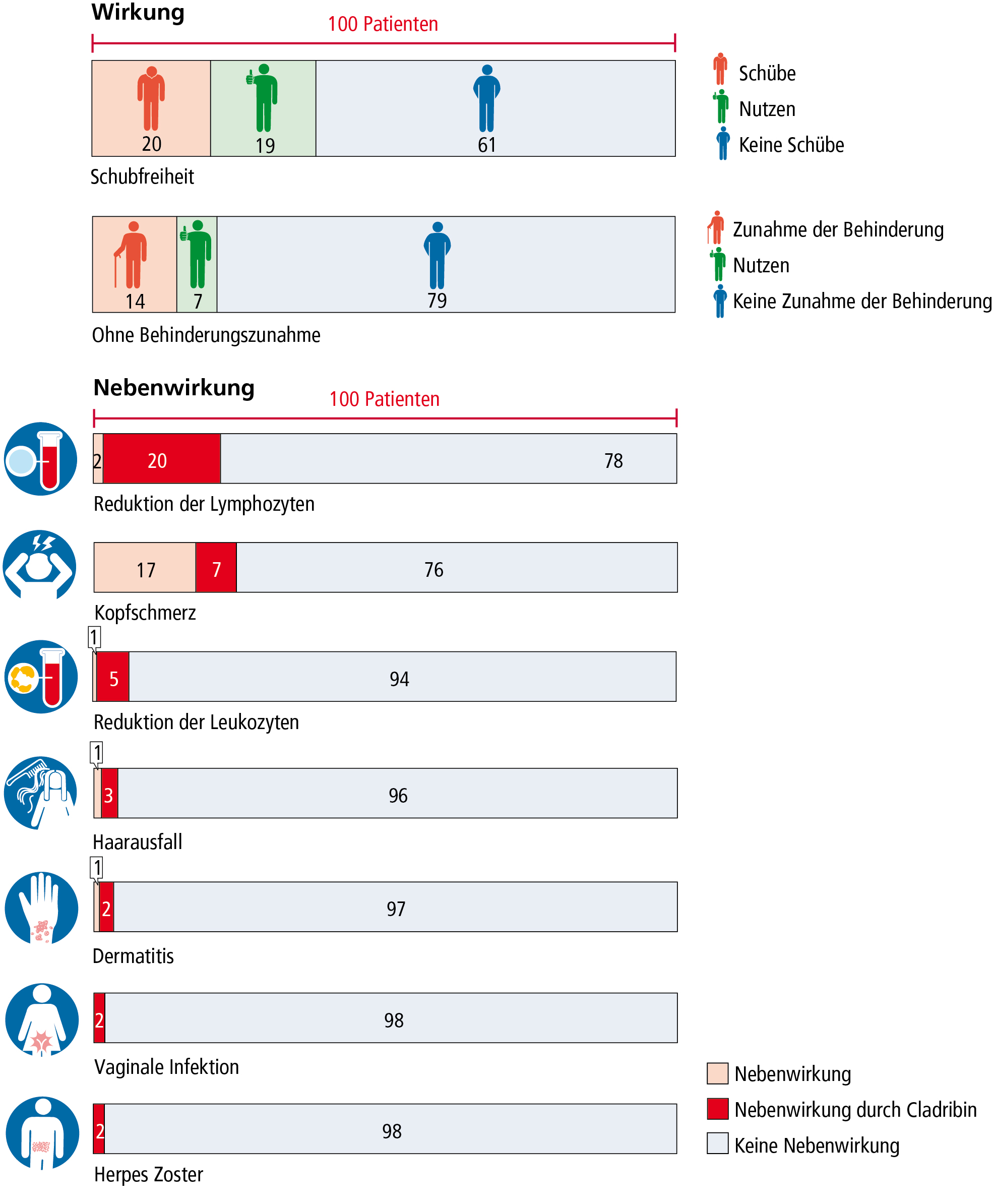
Die Grafik am Kapitelanfang zeigt, wie viele Patienten nach zwei Jahren Therapie mit Cladribin oder Einnahme von Placebo noch schubfrei waren. Daraus kann man den absoluten Nutzen (absolute Risikoreduktion) und den relativen Nutzen (relative Risikoreduktion) berechnen. Die Ergebnisse beziehen sich auf die oben beschriebene Zulassungsstudie CLARITY[90].
Hier wird die Anzahl der Patienten mit Schüben beschrieben. Um Studienergebnisse mit unterschiedlichen Teilnahmerzahlen besser vergleichen zu können, werden die Ergebnisse bezogen auf 100 Patienten dargestellt.
- 80 von 100 Patienten haben einen Nutzen von der Therapie. (Keinen Schub durch die Therapie)
- 20 von 100 Patienten profitieren nicht von der Therapie, da sie trotz der Einnahme von Cladribin einen Schub hatten.
- 61 von 100 Patienten profitieren nicht, da sie auch ohne Cladribin schubfrei geblieben sind.
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl von Patienten mit Schüben unter Cladribin (20) von denen mit Schüben unter Placebo (39) abzieht. Hier profitieren 39– 20, also 19 von 100 Patienten von der Therapie.
2. Wirkung auf die Anzahl der Schübe pro Jahr
Die jährliche Schubrate zeigt, wie viele Schübe durchschnittlich pro Jahr pro Patient auftraten. Sie lag in der Placebo-Gruppe bei 0,33 Schüben gegenüber 0,14 in der Cladribin-Gruppe. Etwas verständlicher ausgedrückt: Die Patienten in der Placebo-Gruppe haben im Durchschnitt alle 3 Jahre einen Schub, die Patienten in der Cladribin-Gruppe nur alle 6,5 Jahre. Die Schubrate in der Placebo-Gruppe ist relativ niedrig. Dies gibt einen Hinweis darauf, dass die Patienten in der Studie generell nur eine geringe Krankheitsaktivität hatten.
3. Wirkung auf die Zunahme der Behinderung
Die Zunahme der Behinderung wurde in den Zulassungsstudien mit Hilfe des EDSS gemessen, einer Behinderungsskala von 0 bis 10 (wobei 0 keiner Behinderung entspricht). Die Grafik am Kapitelanfang zeigt, wie viele Patienten nach zwei Jahren Therapie mit Cladribin oder zweijähriger Einnahme von Placebos keine Zunahme der Beeinträchtigung hatten. Dargestellt ist wieder der absolute Nutzen (absolute Risikoreduktion) und der relative Nutzen (relative Risikoreduktion).
Hier wird die Entwicklung der Behinderung bezogen auf 100 Patienten beschrieben:
- 86 von 100 Patienten haben durch die Einnahme von Cladribin keine Zunahme der Behinderung
- 14 von 100 Patienten haben trotz der Cladribin-Therapie eine Zunahme der Behinderung
- 79 von 100 Patienten profitieren nicht von der Therapie, sie haben unabhängig von der Therapie keine Zunahme der Behinderung.
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl von Patienten mit einer Behinderungszunahme unter Cladribin (14) von denen mit Placebo (21) abzieht. Hier profitieren 21 -14, also 7 von 100 Patienten von der Therapie.
Langzeitwirkung
Im Anschluss an die zweijährige CLARITY-Studie[90] wurde eine sogenannte Extensions-, also Verlaufsstudie durchgeführt (CLARITY EXTENSION), die ebenfalls zwei Jahre andauerte. Es nahmen zwei Drittel (806 von 1326 Patienten) der CLARITY-Studie daran teil. Die beiden Studiengruppen wurden auf drei neue Studiengruppen verteilt: Eine Gruppe mit fortgesetzter Therapie, eine mit Therapiepause und eine mit neuer Therapie. Nach zwei Jahren hatten in den verschiedenen Gruppen 75 bis 81% der Patienten keinen Schub und 73 bis 78% keine Zunahme der Behinderung. Diese Unterschiede zwischen den Gruppen waren nicht signifikant. Das bedeutet, es war egal, ob Patienten zuerst ein Placebo und dann Cladribin, erst Cladribin und dann Placebo oder vier Jahre lang durchgängig Cladribin eingenommen hatten.
Da es keine Gruppe gab, die über die gesamte Zeit von vier Jahren ein Placebo erhalten hat, ist unklar, wie der natürliche Verlauf der MS in dieser Zeit gewesen wäre. Es lässt sich aber sagen, dass eine vierjährige Einnahme von Cladribin nicht besser ist als eine zweijährige. Aus diesem Grund ist die Einnahmezeit von Cladribin vorerst auf zwei Jahre begrenzt.
4. Wirkung auf die MRT/das Kernspin in zwei Jahren
In der MRT treten Kontrastmittelanreicherungen und sogenannte T2-Herde auf, die als Ausdruck der Entzündung bei MS betrachtet werden. Dabei können Herde größer werden oder ganz neu auftreten.
28% der Patienten in der Placebo-Gruppe und 62% in der Cladribin- Gruppe waren über die Studiendauer frei von neuen oder vergrößerten T2-Herden. 47% der Patienten in der Placebo-Gruppe und 87% in der Cladribin-Gruppe hatten über die Studiendauer keine Herde mit Kontrastmittelanreicherungen.
Da Kontrastmittelanreicherungen nur eine Momentaufnahme sind, stellen wir nur die Entwicklung der T2-Herde im Querschnitt eines Gehirns grafisch dar. Dargestellt ist die Anzahl von 100 Patienten ohne bzw. mit neuen oder vergrößerten Herden.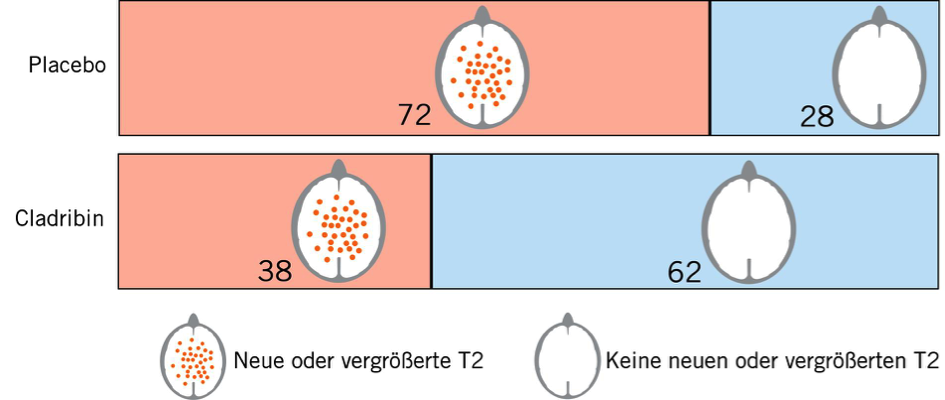
Zulassungsstudien
Die Wirkung von Cladribin auf die Schubrate und die Zunahme der Behinderung wurde in der Zulassungsstudie CLARITY[90] (CLAdRIbine Tablets treating multiple sclerosis orally) geprüft und 2010 veröffentlicht. Eingeschlossen wurden Patienten, die in den 12 Monaten vor Studienbeginn mindestens einen Schub hatten. Insgesamt wurden 1326 Patienten mit aktiver Multipler Sklerose über einen Zeitraum von zwei Jahren untersucht. Langfristige Effekte werden in Therapieregistern untersucht, liefern aber nicht so aussagekräftige Daten wie Zulassungsstudien.
In CLARITY[90] wurde die Wirksamkeit von zwei unterschiedlichen Cladribin-Dosierungen mit Placebo verglichen. Die Darstellung der Ergebnisse bezieht sich auf die zugelassene, niedrigere Dosierung (3.5 mg Cladribin pro Kilogramm Körpergewicht, auch 3.5 mg/kg KG). Die in den Studien ebenfalls getestete höhere Dosierung (5.25 mg/kg KG Cladribin) war insgesamt nicht wirksamer.
Die CLARITY-Studie zeigte eine signifikant überlegene Wirksamkeit des Medikaments gegenüber einer Placebogabe.
Fasst man neue T2-Herde und Kontrastmittel anreichernde Herde als gesamte MRT-Aktivität zusammen, so fanden sich in der Placebo-Gruppe 25% und in der Cladribin-Gruppe 60% ohne MRT-Aktivität.
Im Glossar finden Sie Daten zu dem Anteil der Patienten, bei denen es über 2 Jahre keine Anzeichen einer Krankheitsaktivität gab (NEDA - no evidence of disease activity).
Welche Nebenwirkungen hat Cladribin?
Bei wie vielen Patienten traten Nebenwirkungen auf?
In der Zulassungsstudie CLARITY[90] hatten 347 (81%) der Patienten in der Cladribin-Gruppe Nebenwirkungen und 319 (73%) der Patienten in der Placebo-Gruppe. Dieser Unterschied war statistisch signifikant.
Grundsätzlich ist wichtig zu wissen, dass Nebenwirkungen in Studien nicht nur bei den Patienten auftreten, die ein neues Medikament erhalten, sondern auch in der Studiengruppe mit einem bekannten Medikament oder Placebo.
Bei wie vielen Patienten führten die Nebenwirkungen zum Therapieabbruch?
Bei 9 (2%) Patienten in der Placebo-Gruppe und bei 15 (3,5%) in der Cladribin-Gruppe führten die Nebenwirkungen zum Abbruch der Behandlung. Dieser Unterschied war jedoch nicht statistisch signifikant.
Häufige Nebenwirkungen
In der Tabelle sind Nebenwirkungen aufgeführt, die aus der Studie CLARITY[90] berichtet wurden und bei mindestens 2% der Patienten auftraten. Angegeben ist die Patientenzahl von 100 Patienten. In der Grafik zu Anfang des Kapitels sowie in der Faktenbox weiter unten werden jedoch lediglich die wichtigsten Nebenwirkungen dargestellt.
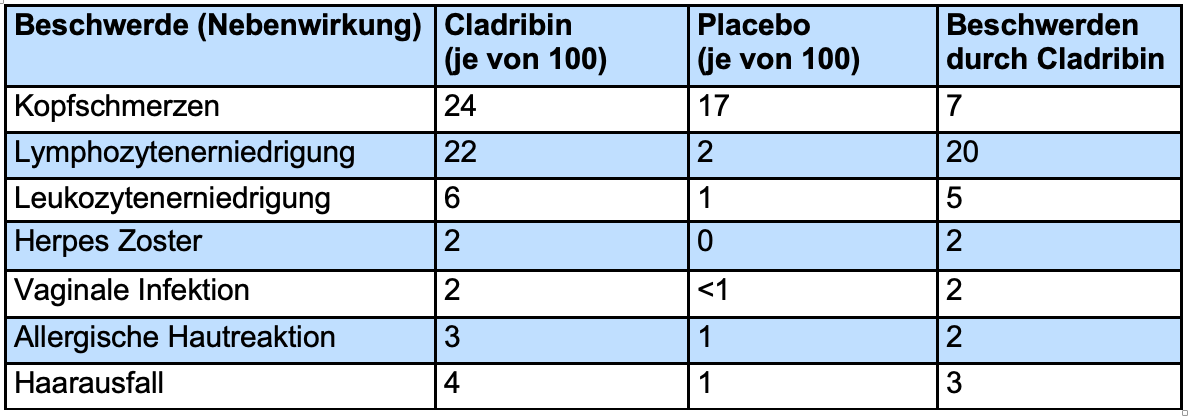
Kopfschmerzen traten in der Placebo-Gruppe bei 17%, in der Cladribin-Gruppe bei 24% auf, sprich es gab einen Unterschied von 7%.
Eine deutliche, jedoch vorübergehende Verminderung der Zahl der Lymphozyten [unter 500 Zellen pro Mikroliter (μl)] trat bei 20 von 100 Patienten nach Cladribin-Gabe auf und ist durch den Wirkmechanismus des Medikaments bedingt. Am Ende der zweijährigen Therapiestudie lag der Wert im Mittel bei 900 Zellen/μl, also knapp unter dem Normbereich von 1500-300 μl. Auch eine vorübergehende Erniedrigung der Gesamtzahl der weißen Blutkörperchen (Leukozyten) unter 3.000 Zellen/μl war in der Cladribin-Gruppe mit 5 von 100 Patienten häufiger als in der Placebo-Gruppe. Dennoch kam es insgesamt nicht gehäuft zu Infektionen. Allerdings litten mehr Patienten in der Cladribin-Gruppe unter einem Herpes zoster (Gürtelrose) (2 von 100) sowie vaginalen Infektionen (2 von 100).
Zusätzlich trat bei 2 von 100 Patienten in der Cladribin-Gruppe eine allergische Hautreaktion (allergische Dermatitis) auf und bei 2 von 100 kam es zu Haarausfall.
Schwere Nebenwirkungen und Todesfälle
In diesem Abschnitt werden nicht nur die schweren Nebenwirkungen (z.B. lebensbedrohliche Erkrankungen) berichtet, die unter der heute zugelassenen Cladribin-Dosis von 3,5mg pro kg Körpergewicht (KG) auftraten, sondern auch die, die bei der höheren getesteten Gesamtdosis von insgesamt 5,25 mg / kg Körpergewicht (KG) auftraten.
In der Placebo-Gruppe kam es bei 6,4%, in der Cladribin-Gruppe bei 8,7% der Patienten zu schweren Nebenwirkungen, d. h. sie kamen bei Cladribin-Einnahme nicht gehäuft vor.
Während und nach der Studie traten insgesamt 6 Todesfälle auf, jeweils 2 in jeder Behandlungsgruppe. Die Ursachen waren:
- in der Placebo-Gruppe ein Suizid und ein Schlaganfall
- in der 3,5 mg / kg KG-Cladribin-Gruppe ein Herzinfarkt und ein Tod aufgrund einer Bauchspeicheldrüsenkrebserkrankung nach Studienende
- in der 5,25 mg / kg KG-Cladribin-Gruppe: ein Todesfall durch Ertrinken und einer durch einen Herzinfarkt nach Studienende
Krebserkrankungen
Während der Zulassungsstudie (CLARITY[90]) traten bei den Patienten, die 3,5 mg / kg Körpergewicht Cladribin erhielten, 3 bösartige Tumore auf: 1 Bauchspeicheldrüsenkrebs, 1 Melanom (schwarzer Hautkrebs) und 1 Eierstockkrebs.
Nach der Studie erkrankte eine Patientin der 5,25 mg / kg Körpergewicht-Cladribin-Gruppe an einem Krebs, der sich bei einer Schwangerschaft am Mutterkuchen bilden kann. In der Placebo-Gruppe traten keine Krebserkrankungen auf.
In der Studie mit ersterkrankten Patienten (ORACLE) trat bei 5,25 mg / kg Cladribin ein Gebärmutterkrebs auf, bei 3,5 mg / kg Cladribin 1 Schilddrüsenkrebs und 2 Hauttumore. Bei Placebo-Gabe traten 3 gutartige Schilddrüsentumore auf.
Statistisch gesehen traten die Krebserkrankungen bei Cladribin-Tabletten-Einnahme nicht gehäuft auf. Dennoch ist zu beachten, dass alle Medikamente, die das Immunsystem beeinflussen, das Krebsrisiko erhöhen können. Dies kann aber nur in Langzeitstudien geklärt werden.
Infektionen
Wenn man alle Arten von Infekten zusammenzählt, traten diese bei Cladribin-Gabe nicht häufiger auf als bei den Patienten, die ein Placebo erhielten. Es kam jedoch bei einer Patientin zu einer Reaktivierung einer nicht bekannten Tuberkulose.
In der Therapie der Haarzellleukämie mit Cladribin wurden Fälle einer gefährlichen Gehirnentzündung, der Progressiven Multifokalen Leukenzephalopathie, kurz PML, berichtet. Bei MS-Patienten gab es bisher, in 12 Jahren klinischer Erfahrung, nach Cladribin-Gabe aber keine PML-Fälle.
Dennoch ist zu beachten, dass alle Medikamente, die das Immunsystem beeinflussen, auch das Infektionsrisiko erhöhen können. Wenn die Lymphozyten unter eine bestimmte Schwelle sinken (< 200 Zellen/μl), wird daher auch eine vorbeugende Herpesvirustherapie empfohlen (siehe unten).
Welche neuen Nebenwirkungen wurden nach Abschluss der Zulassungsstudien berichtet?
Neue Nebenwirkungen wurden bisher nicht berichtet. In der Verlaufsstudie, bei der ein Teil der Patienten bis zu vier Jahre am Stück mit Cladribin behandelt wurde, bestätigten sich die bekannten Nebenwirkungen. Bis dahin unbekannte Nebenwirkungen traten nicht auf.
Worauf muss bei der Therapie mit Cladribin geachtet werden?
Unter welchen Umständen sollte Cladribin nicht eingenommen werden?
Cladribin sollte nicht eingenommen werden bei
- einer Überempfindlichkeit gegenüber dem Wirkstoff.
- akuten Infektionen.
- chronischen Infektionen wie HIV, Hepatitis-B oder -C (HBV und HCV) oder Tuberkulose.
- einer Immunschwäche oder einer Therapie mit einem Medikament, welches das Immunsystem verändert bzw. unterdrückt.
- aktiven Krebserkrankungen.
- einer mittelschweren oder schweren Einschränkung der Nieren- oder Leberfunktion.
- Schwangerschaft oder in der Stillzeit.
- Fruktoseintoleranz, da die Tablette Sorbitol enthält.
Welche Sicherheitsabstände müssen eingehalten werden?
Bei Patienten, die bereits eine Therapie erhalten haben, die das Immunsystem beeinflusst oder hemmt, müssen Sicherheitsabstände vor Umstellung auf Cladribin eingehalten werden. Diese richten sich nach der Wirkdauer der Medikamente. Die Wartezeit beträgt nach der Behandlung mit ...
- Fingolimod und Teriflunomid (nach Auswaschung!) mindestens 4 Wochen.
- Natalizumab und Daclizumab mindestens 6 – 8 Wochen.
- Azathioprin, Ciclosporin A, Cyclophosphamid, Methotrexat und Mitoxantron mindestens 3 Monate.
- Alemtuzumab, Ocrelizumab und Rituximab mindestens 6 – 12 Monate.
Bei der vorherigen Verwendung von Interferonen, Glatirameracetat oder Dimethylfumarat müssen, solange sich etwaige Blutbildveränderungen normalisiert haben, keine Sicherheitsabstände eingehalten werden.
Worauf ist bei Therapiebeginn zu achten?
Weil Cladribin das Immunsystem hemmt, sollten vor Therapiebeginn alle Standardimpfungen durchgeführt werden, die die STIKO (Ständige Impfkommission) für Menschen empfiehlt, deren Immunsystem teilweise blockiert werden soll.
Falls der Antikörperschutz gegen Windpocken (VZV) im Blut nicht ausreicht, sollte vor Beginn der Therapie eine Impfung erfolgen. Die Therapie mit Cladribin-Tabletten sollte erst nach erfolgreicher Impfung, frühestens nach 4 – 6 Wochen begonnen werden.
Was muss während der Therapie kontrolliert werden?
Das Krankheitsbezogene Kompetenznetz Multiple Sklerose (KKNMS) empfiehlt: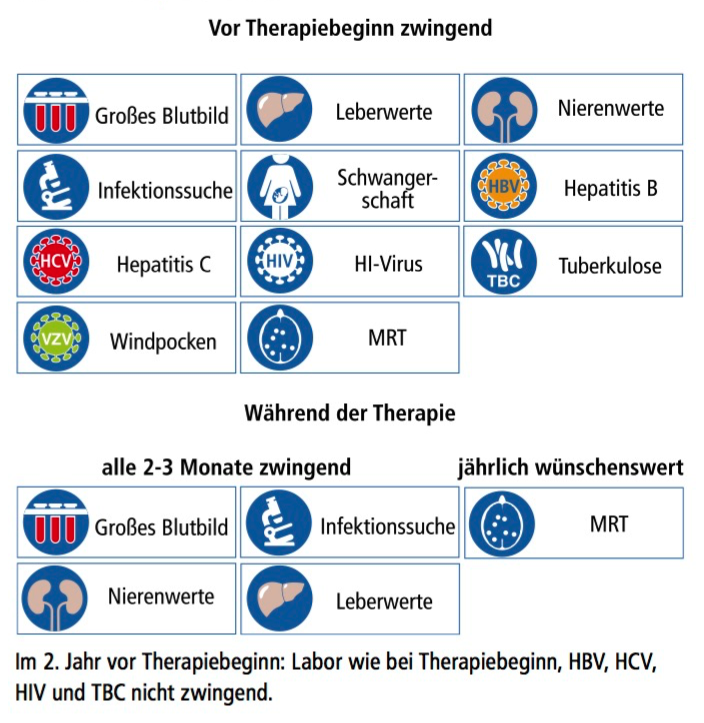
Kontrolle der Leuko- und Lymphozytenzahl
Vor Beginn einer Therapie mit Cladribin muss ein großes Blutbild, das heißt die Bestimmung der Anzahl aller Blutzellen, erfolgen. Damit man mit der Einnahme von Cladribin beginnen bzw. diese im zweiten Jahr fortsetzen kann, müssen die Leukozyten und Lymphozyten, die weißen Blutzellen also, über bestimmten Grenzwerten liegen. Ist die Anzahl geringer, kann die Behandlung um bis zu sechs Monate verschoben werden. Sollten die Werte weiter niedrig bleiben, muss die Therapie abgesetzt werden.
Patienten, deren Lymphozytenzahl während der Cladribin-Behandlung unter einen Grenzwert von 500 Zellen/μl sinkt, sind anfälliger für eine Herpes-Infektion. Eine vorbeugende medikamentöse Herpes-Therapie mit Aciclovir-Tabletten sollte ab einem Wert von 200 Zellen/μl eingeleitet werden. Wegen des Risikos anderer Infektionen sollten diese Patienten generell aktiv überwacht und gegebenenfalls behandelt werden. Während der Behandlungsdauer und auch in den Folgejahren wird empfohlen, die Standard-Krebsvorsorgeuntersuchungen wahrzunehmen.
Cladribin - Häufig gestellte Fragen
Wirkt Cladribin besser oder schlechter als andere MS-Medikamente?
Hierzu liegen derzeit noch keine Daten aus vergleichenden Studien vor.
Wie lange wird behandelt?
Die Behandlungsdauer mit Cladribin-Tabletten ist für zwei Jahre vorgesehen mit anschließenden zwei Jahren ohne Therapieeinnahme. Die Langzeitdaten der Zulassungsstudie sprechen dafür, dass der Effekt zumindest zum Teil zwei weitere Jahre anhält. Über diese Zeit hinaus liegen keine Daten vor. Nutzen und Risiko der Einnahme müssen laufend überprüft werden. Ein Abschätzen des Nutzens ist oft frühestens nach einem Jahr möglich. Als Hinweise für eine Wirksamkeit werden allgemeine Schubfreiheit und das Fehlen neuer Herde in der MRT angesehen.
Deshalb empfiehlt das KKNMS eine Ausgangs-MRT und anschließend jährlich eine MRT, um Nutzen und auch mögliche Risiken abzuschätzen.
Schwangerschaft und Stillzeit
Cladribin darf in der Schwangerschaft und Stillzeit nicht eingenommen werden. In Tierstudien und an menschlichen Zellen in Laborversuchen zeigte Cladribin eine schädigende Wirkung auf den Embryo.
Bevor eine Behandlung mit Cladribin begonnen wird, muss deshalb eine Schwangerschaft ausgeschlossen werden. Frauen und Männer, die mit Cladribin behandelt werden, sollten während der Behandlung und bis 6 Monate danach nicht schwanger werden bzw. keine Kinder zeugen.
Es besteht die Möglichkeit, dass Cladribin die Wirkung hormoneller Verhütungsmittel (z.B. der Pille) beeinträchtigt. Frauen, die eine solche Methode anwenden, müssen während der Tage, an denen Cladribin eingenommen wird, und in den 4 Wochen danach zusätzlich noch eine „Barrieremethode“, also z.B. Kondome, benutzen.
Auch nach dieser Zeit müssen Patientinnen sowie Patienten und ihre Partnerinnen weiterhin zuverlässig verhüten, es reicht jedoch eine einzelne Verhütungsmethode (z.B. Pille oder Kondom).
Sollte während der Cladribin-Therapie trotzdem eine Schwangerschaft eintreten, kann dies zu einer Fehlgeburt oder Fehlbildungen führen. Eine eventuelle Einnahme von Cladribin sollte sofort unterbrochen werden.
6 Monate nach der letzten Einnahme von Cladribin ist nicht mehr von einem Risiko für eine neue Schwangerschaft auszugehen.
Es ist nicht bekannt, ob Cladribin in die Muttermilch übertritt. Sicherheitshalber sollte auf das Stillen während der Einnahme von Cladribin und bis zu 6 Monate nach der letzten Einnahme verzichtet werden.
Verlauf von Schwangerschaften in der Zulassungs- und Verlängerungsstudie (Verlinkungen)
Im gesamten Studienprogramm wurden 44 Schwangerschaften bei Patientinnen gemeldet, die Cladribin einnahmen, und 20 in der Placebo-Gruppe.
4 Patientinnen in der Placebo-Gruppe sowie 14 Patientinnen in den Cladribin-Gruppen entschieden sich für eine Abtreibung. Fehlgeburten traten in den Behandlungsgruppen nicht häufiger auf als in der Placebo-Gruppe. Bei keinem der Kinder, die zur Welt kamen (9 in der Placebo-Gruppe, 18 in den Cladribin-Gruppen), wurden Fehlbildungen gemeldet.
Zusätzlich kam es in der Placebo-Gruppe zu einer Entwicklungsstörung des Fötus mit Ablösung des Mutterkuchens.
In den Behandlungsgruppen trat bei einer Schwangerschaft ein Chorionkarzinom, d.h. eine bösartige Veränderung am Mutterkuchen, auf sowie zwei Eileiter Schwangerschaften.
Impfungen
Umfassende Untersuchungen zu Impfungen und Cladribin-Tabletten liegen nicht vor. Eine Beeinträchtigung des Impferfolgs kann nicht ausgeschlossen werden. Insofern sollten alle von der STIKO (Ständige Impfkommission) für Patienten mit einem eingeschränkten Immunsystem empfohlenen Impfungen vor Therapiebeginn durchgeführt bzw. aufgefrischt werden.
Sogenannte Lebendimpfstoffe, bei denen lebende, aber unschädlich gemachte Erreger verwendet werden, müssen möglichst vermieden werden. Cladribin-Patienten haben möglicherweise keine ausreichende Abwehr und könnten durch die eigentlich harmlosen Impferreger krank werden.
Infektionen
Wenn eine Infektion zum Zeitpunkt der Behandlungsphase besteht, sollte diese erst nach Ausheilen der Infektion begonnen werden.
Welche Alternativen bestehen zu Cladribin?
Cladribin ist nur eine von verschiedenen zugelassenen MS-Therapien. Eine Übersicht finden Sie auf der Hauptseite. Systematische Vergleichsstudien von Cladribin mit anderen MS-Medikamenten wurden bislang nicht durchgeführt.
Eine weitere Möglichkeit ist auch, (noch) keine Immuntherapie durchzuführen. Ohne Therapie folgt die MS dem natürlichen Verlauf. Wie dieser zumindest kurzfristig aussieht, kann man aus den Daten der Placebo-Gruppe in der Zulassungsstudie[90] abschätzen: Über zwei Jahre blieben in der Placebo-Gruppe 61 von 100 Patienten schubfrei und 79 von 100 ohne Zunahme der Beeinträchtigung.
Cladribin - Alles auf einen Blick