Ozanimod (Zeposia®)
Das Präparat reduziert bei einem Teil der Patienten die Schubrate und hält die Behinderungszunahme auf.
Als häufige Nebenwirkungen treten eine Entzündung des Nasen-Rachen-Raums und eine verminderte Anzahl der weißen Blutkörperchen auf (mehr dazu unter Nebenwirkungen). Zudem können ein erhöhter Blutdruck und erhöhte Leberwerte mit der Einnahme einhergehen. Eine regelmäßige Blutuntersuchung sollte daher zur Überwachung durchgeführt werden.
Wirkungen und Nebenwirkungen im graphischen Überblick
Schubfreie Patienten


Patienten ohne Zunahme einer Behinderung
12 von 100 Patienten zeigten über 2 Jahre Studeinzeit eine Zunahme der Behinderung.
Nebenwirkungen

Was ist Ozanimod?
Ozanimod ist die Weiterentwicklung des 2011 zugelassenen Immunmedikament Fingolimod (Gilenya® ).
Wie wirkt Ozanimod?
Das Medikament bindet an die Bindungsstelle des sogenannten Sphingosin-1-Phosphat-Rezeptors, der in vielen Geweben des Körpers vorhanden ist. Im Gegensatz zu Fingolimod bindet Ozanimod nur an bestimmte Untergruppen und verursacht weniger Nebenwirkungen am Herzen.
Lymphozyten (weiße Blutkörperchen) werden gehindert, aus den Lymphknoten in das Bkut zu wandern. Weniger Lymphozyten gelangen in das Nervensystem und können dieses weniger schädigen. Es findet also eine Umverteilung (nicht Zerstörung) der Lymphozyten statt.
Für wen ist Ozanimod zugelassen?
Seit Mai 2020 ist Ozanimod von der europäischen Zulassungsbehörde (EMA) zur Therapie des schubförmig-remittierendem Verlauf der Multiple Sklerose bei erwachsenen MS-Betroffenen zugelassen.
Empfohlen wird es bei aktiver RRMS, definiert durch klinische oder bildgebende Befunde. Der Verlauf einer MS gilt als entzündlich aktiv, wenn unter einer Immuntherapie
- mindestens ein klinisch eindeutig objektivierbarer Schub oder
- ein klinischer Schub mit mindestens einer neuen typischen Läsion in der MRT oder
- bei schubfreien Betroffenen zu mindestens 2 Zeitpunkten mindestens eine neue MS-typische Läsion in der MRT in einem Zeitraum von bis zu 2 Jahren nachweisbar ist.
Wie wird Ozanimod eingenommen?
Das Medikament wird 1xtäglich als Kapsel oral eingenommen.
Im Unterschied zu Fingolimod wir Ozanimod langsam bis zur Zieldosis von 0,92mg gesteigert. Ein einschleichen könnte so aussehen:
- Behandlungstag 1-4: 1xtgl 0,23mg
- Behandlungstag 5-7: 1xtgl 0,46mg
- ab Behandlungstag 8: 1xtgl 0,92mg
Die Zieldosis von 0,92mg entspricht der Darreichungsform von 1mg Ozanimod-HCl, eine halbe Dosis Ozanimod (0,46mg) entspricht demnach 0,5mg Ozanimod-HCl.
Um es zu vereinfachen, wir auf den nächsten die Dosierung auf 1mg (=0,92mg) und 0,5mg (=0,46mg) Ozanimod-HCl bezogen.
Sollte die Einnahme vergessen werden, wird die Therapie mit der nächsten Dosis nach Plan fortgesetzt. Zu Behandlungsbeginn sollte bei Patienten mit Vorerkrankung des Herzens das Herz-Kreislauf-System für 6 Stunden überwacht werden.
Wird die Therapie unterbrochen, sollte die Erstgabe überwacht und ggf. neu eindosiert werden. Dies gilt für folgende Unterbrechungen: 1 Tag während der ersten 2 Behandlungswochen, >7 Tage während der 3. und 4. Behandlungswoche, >2 Wochen nach einem Behandlungsmonat.

Bildquelle: https://www.shop-apotheke.com/arzneimittel/16151959/zeposia-0-92-mg.html, letzter Zugriff: 30.06.2021
Wie wirksam ist Ozanimod bei schubförmiger MS?
SUNBEAM untersuchte über 1 Jahr 1346 Patienten, RADIANCE über 2 Jahre 1320 Patienten. Für den Einschluss in die Studie galten folgende Voraussetzungen:
- in dem Jahr vor Studienbeginn mindestens ein stattgefundenes Schubereignis oder
- in den 2 Jahren vor Studienbeginn mindestens einen Schub und eine aktive Läsion in der MRT
Der EDSS-Wert der Patienten lag zwischen 0 und 5,0. Beobachtet und verglichen wurde zwischen 3 Gruppen: Eine erhielt 30µg Interferon beta-1a, eine täglich 1mg Ozanimod, die dritte täglich 0,5mg Ozanimod.
Da sich die Studie SUNBEAM nur auf 1 Jahr bezieht, werden im Folgen die Ergebnisse der Studie RADIANCE dargestellt. Die dargestellte Gruppe erhielt 1mg Ozanimod (= Ozanimod HCl, dies entspricht 0,92mg Ozanimod)
Wirkung auf die Schubfreiheit
Die folgende Grafik zeigt, wie viele Patienten nach 2 Jahren Therapie mit Ozanimod oder Einnahme von Interferon noch schubfrei waren. Daraus kann man den absoluten Nutzen (absolute Risikoreduktion*) und den relativen Nutzen (relative Risikoreduktion*) berechnen:
von 100 Patienten, die Interferon erhielten, erlitten 34 einen Schub
von 100 Patienten, die Ozanimod erhielten, erlitten 24 einen Schub
Der absolute Nutzen entspricht 34-24 = 10, der relative Nutzen entspricht 10/34= 0,29 -> 29%

Wirkung auf die Anzahl der Schübe pro Jahr
Die jährliche Schubrate zeigt, wie viele Schübe durchschnittlich pro Jahr pro Patient auftraten. In der RADIANCE-Studie lag sie in der Interferon-Gruppe bei 0,28 Schüben gegenüber 0,22 bzw. 0,17 in der Ozanimod-Gruppe bezogen auf eine Therapiedosis von 0,5mg respektive 1 mg Ozanimod.
Etwas verständlicher ausgedrückt: Die Patienten in der Interferon-Gruppe haben im Durchschnitt circa alle 3,6 Jahre einen Schub, die Patienten in der Ozanimod-Gruppe nur circa alle 4,5 bzw. alle 5,9 Jahre.
Wirkung auf die Behinderungszunahme
Die Zunahme der Behinderung (Behinderungsprogression) wurde in den Zulassungsstudien mit Hilfe des EDSS gemessen, einer Behinderungsskala von 0 bis 10 (wobei 0 keiner Behinderung entspricht).
Hier konnte kein Unterschied zur Interferon-Gruppe gezeigt werden.
In beiden Gruppen zeigten 12 von 100 Patienten über 2 Jahre Studie eine Zunahme der Beeinträchtigung.
Wirkung auf die MRT in zwei Jahren
In der MRT treten Kontrastmittelanreicherungen und so genannte T2-Herde auf, die als Ausdruck der Entzündung bei MS betrachtet werden. Dabei können Herde größer werden oder ganz neu auftreten.
18 % der Patienten in der mit Interferon behandelten Gruppe und 24 % der Patienten in der Ozanimod-Gruppe blieben über die Studiendauer frei von neuen oder vergrößerten T2-Herden.
56 % der Patienten in der mit Interferon behandelten Patientengruppe und 66 % in der Ozanimod-Gruppe hatten über die Studiendauer keine Herde mit Kontrastmittelanreicherungen.

Welche Nebenwirkungen hat Ozanimod?
Wie bereits beschrieben, untersuchte die Studie über den Zeitraum von 2 Jahren die Wirkung von Ozanimod in Referenz zu der Wirkung Interferons.
Bei wie vielen Patienten traten Nebenwirkungen auf?
- In der Ozanimodgruppe zeigten 324 von 434 Patienen (75%) Nebenwirkungen.
- In der Interferongruppe zeigten 365 von 550 Patienten (83%) Nebenwirkungen.
Bei vielen Patienten führten die Nebenwirkungen zum abbruch der Behandlung?
- In der Ozanimodgruppe fürhten bei 13 Patienten (3,0%) die Nebenwirkungen zum Abbruch der Behandlung
- In der Interferongruppe führten bei 18 Patienten (4,1%) die Nebenwirkungen zum Abbruch der Behandlung.
In der folgenden Grafik ist, bezogen auf 100 Patienten, dargestellt, wie viel häufiger Nebenwirkungen in der Ozanimod-Gruppe als in der Interferon-Gruppe auftraten.
Die Darstellung der Nebenwirkungen folgt grundsätzlich der Analyse der über zwei Jahre durchgeführten Zulassungsstudie RADIANCE mit Bezug auf die zugelassene Dosis von 1 mg Ozanimod. Auffällige Befunde der Einzelstudien RADIANCE und SUNBEAM, aber auch auffallende Nebenwirkungen unter den nicht zugelassenen 0,5 mg werden zusätzlich berichtet.

Grafik: Zur Veranschualichung werden die Ergebnisse auf 100 Patienten bezogen
Obere Atemwegsinfektionen
Der Begriff 'obere Atemwegsinfektionen' beschrieb in der Studie Infektionen des Nasen-Rachen-Raums (Nasopharyngitis), des Rachens (Pharyngitis) und der Nase (Rhinitis). Allgemein traten obere Atemwegsinfektionen signifikant häufiger bei Patienten mit Ozanimod-Therapie als bei Patienten ind der mit Interferon behandelten Gruppe auf. 68 Patienten (16 %) der Ozanimod-Gruppe berichteten über eine Nasopharyngitis, in der Interferongruppe nur 48 Patienten (11 %).
Leberwerterhöhung
Ein häufig genutzter Leberwert, die sogenannte Alanin-Aminotransferase (auch ALT, ALAT oder GPT abgekürzt), erreichte bei 6% der Ozanimod-Gruppe (26 Patienten) und 4% der Interferon-Gruppe (20 Patienten) Werte, die das 3-fache der normalen Obergrenze betrugen. Dieser Unterschied war signifikant. Die Leberwerterhöhung war meist vorübergehend auch ohne Pausierung der Medikation.
Das Enzym γ-Glutamyltransferase (γGT) ist ein weiterer häufig genutzter Marker für die Funktion der Leber, sowie der Gallenblase. DIe Studie RADIANCE zeigte bei 6% der Ozanimod-Gruppe erhöhte Werte, in der Interferon-Gruppe nur bei 2%.
Bluthochdruck
Bei 24 der Ozanimod Patienten (6 %) und 14 der mit Interferon behandelten Patienten (3 %) wurden geringe Blutdruckerhöhungen beobachtet. Dieser Unterschied war nicht signifikant.
Harnwegsinfektionen
In RADIANCE traten zahlenmäßig mehr Harnwegsinfekte in den Ozanimod-Gruppen als in der Interferon-Gruppe auf. Die Unterschiede waren nicht signifikant.
Rückenschmerzen
Ein Teil der Patienten bemerkte Rückenschmerzen. Die Differenz war zwischen den Gruppen nicht signifikant.
In RADIANCE gaben 18 Patienten (4 %) aus der Ozanimod-Gruppe und 14 Patienten (3 %) aus der Interferon-Gruppe im 24-Monate dauernden Studienzeitraums Rückenschmerzen an.
Gelenkschmerzen
In RADIANCE traten in der Ozanimod-Gruppe vermehrt Gelenkschmerzen auf. 15 Patienten (3,5 %) klagten in der Ozanimod-Gruppe über Gelenkschmerzen, dagegen nur 6 Patienten (1,4 %) in der Interferon-Gruppe. Dies war statistisch signifikant.
Herzschlagverlangsamung
Eine Verlangsamung des Herzschlags (medizinisch: Bradykardie) wurde ausschließlich in den ersten Stunden nach Gabe des Medikaments nachgewiesen. Durchschnittlich betrug diese in der RADIANCE Studie eine Verlangsamung um 0,6 Schläge pro Minute. In der RADIANCE Studie kam es bei 4 Patienten (<1 %) der Ozanimod-Gruppe und keinem Patienten der Interferon-Gruppe zu einer Bradykardie unter 45 Schläge pro Minute, Diese bildete sich nach 7 Stunden wieder zurück.
Die Verlangsamung der Herzfrequenz fällt im Gegensatz zu dem anderen zugelassenen Sphingosinphosphat-1-Modulator Fingolimod deutlich geringer aus. Das liegt zum einen am spezifischeren Wirkmechanismus, der weniger Wirkung auf das Herz aufweist, zum anderen an der einschleichenden Dosierung von Ozanimod.
Augenhintergrundveränderungen
Eine Veränderung des Augenhintergrunds mit Wassereinlagerung in der Netzhautmitte an der Stelle des schärfsten Sehens (medizinisch: Makulaödem), kam in RADIANCE und SUNBEAM unter Ozanimod-Therapie in insgesamt 5 Fällen, in der Interferon-Gruppe in 3 Fällen vor. Diese Nebenwirkung war sowohl bei der Dosierung von 1 mg als auch 0,5 mg Ozanimod aufgetreten.
Die Veränderungen normalisierten sich in der Regel 1 bis 6 Monate nachdem die Therapie beendet wurde. Bei Patienten mit Vorerkrankungen wie Diabetes mellitus oder anderen Erkrankungen der Netzhaut in der Vorgeschichte sollte eine Kontrolle des Augenhintergrundes sowohl vor Beginn mit Ozanimod, als auch ca. 3-4 Monate nach Beginn der Einnahme stattfinden, um diese seltene, aber ernsthafte Nebenwirkung zu entdecken
Verminderung der Lymphozytenzahl im Blut
Durch den Wirkmechanismus von Ozanimod kann die Zahl freier Lymphozyten im Blut erniedrigt sein. Diese zeigte sich in den ersten drei Monaten nach Therapiebeginn und blieb im Anschluss weitestgehend stabil.
Eine Erniedrigung der Lymphozytenzahl unter bestimmte Normwerte wird Lymphopenie genannt. Es gab in RADIANCE 18 Patienten (4,2 %) in der Ozanimod-Gruppe mit 1 mg gegenüber keinem Patienten der Interferon-Gruppe, die erniedrigte Lymphozyten unter 200 Zellen pro Mikroliter aufwiesen. Eine Reduktion der Lymphozyten unter 500 pro Mikroliter trat jedoch bei 249 (57,8%) der Ozanimod-Gruppe mit 1 mg auf, in der Interferon-Gruppe dagegen nur bei 6 Patienten (1,4%). Dieser Unterschied war signifikant.
Nach Übereinkunft von MS-Spezialisten und Behörden wurde der untere Grenzwert für Lymphozyten unter Ozanimod-Therapie auf über 200 pro Mikroliter festgelegt. Wird dieser Wert auch nach Therapiepause und erneuter Gabe wieder unterschritten, muss Ozanimod abgesetzt werden. Es ist dabei aber zu bedenken, dass die im Blut gemessene Anzahl der Lymphozyten nur einen groben Anhaltspunkt darüber geben kann, ob die Abwehrfunktionen des Immunsystems intakt sind.
Schwere Infektionen
Es kam in RADIANCE und SUNBEAM nicht signifikant häufiger zu schweren Infektionen bei der Behandlung mit Ozanimod im Gegensatz zur Therapie mit Interferon-beta 1a.
Schwere Infektionen mit Erregern, die typisch für Patienten mit geschwächtem Immunsystem sind, traten nicht auf. Lokale Infektionen mit Herpesviren traten in beiden Gruppen auf. In RADIANCE wurde in der Ozanimod-Gruppe mit 1 mg Dosierung in 4 Fällen Herpes zoster nachgewiesen, in der geringeren Dosis mit 0,5 mg Ozanimod und in der Therapie mit Interferon-beta 1a jeweils in zwei Fällen. Schwere Infektionen mit Herpesviren wurden nicht nachgewiesen.
Auch nach Markteinführung sind bisher keine schweren Infektionen mit Herpesviren bekannt.
Posteriores reversible Enzephalopathie-Syndrom (PRES)
Das PRES ist ein Beschwerdekomplex, der durch plötzliches Auftreten von starkem Kopfschmerz, Verwirrtheit, Krampfanfällen und Sehstörungen gekennzeichnet ist. Die Symptome eines PRES bilden normalerweise zurück, können sich aber auch zu einem Schlaganfall oder einer Hirnblutung entwickeln.
In der Studie RADIANCE wurde über einen Fall von PRES bei einem Patienten aus der Ozanimod-Gruppe berichtet. Dies trat 10 Monate nach Beginn der Therapie auf und war nach Absetzen von Ozanimod rückläufig. Bei Verdacht auf ein PRES ist die Behandlung mit Ozanimod abzusetzen.
Schwere Nebenwirkungen und Todesfälle
Durch Ozanimod bedingte schwere Nebenwirkungen traten in den Studien statistisch nicht gehäuft auf. Es kam sowohl in SUNBEAM als auch RADIANCE und in Verlängerungsstudien zu keinem Todesfall.
Krebserkrankungen
Alle Krebsarten, die in den Zulassungsstudien neu auftraten, waren: Brustkrebs (3 Patienten der Ozanimod-Gruppen, keine Patienten in der Interferon-Gruppen) und verschiedene Hautkrebse (3 Patienten mit Basalzellkarzinom sowie 1 Patient mit einem andersartigen Hautkrebs in den Ozanimod-Gruppen). Demgegenüber fand sich 1 Patient mit einem Basalzellkarzinom in der Interferon-beta 1a-Gruppe. Zusätzlich trat in den Ozanimod-Gruppen ein Hodenkrebs auf. Außerdem gab es einen Patienten in der Interferon-Gruppe, der einen Lymphdrüsenkrebs entwickelt hat.
Welche Nebenwirkungen wurden nach Beendigung der Studie berichtet?
Bisher sind keine neuen Nebenwirkungen beschrieben worden (Stand April 2021).
Was ist bei der Einnahme von Ozanimod zu beachten?
Ozanimod wird mit einem Einschleichschema über 7 Tage langsam eindosiert. Täglich wird eine Kapsel eingenommen: Tag 1-3 0,23mg, ab Tag 4 0,46mg. Wenn keien Nebenwirkungen auftreten, kann ab Tag 8 die Erhaltungsdosis von 0,92mg eingenommen werden.
Bestehen keine Herzerkankungen, ist keine Überwachung bei Erstgabe nötig. Bei Patienten mit bekannter Herzfrequenzverlangsamung (medizinisch: Bradykardie), leichten Herzrhythmusstörungen (keine Kontraindikation!) oder früherer Herzbeschwerden sollte Ozanimod unter einmaliger 6-stündiger Überwachung des Herzens begonnen werden. Hierbei werden Blutdruck, Rhythmus und Herzfrequenz stündlich kontrolliert. Nachdem am Ende der 6 Studnen ein weiteres EKG geschrieben wurde, darf der Patient nachhause entlassen werden.
Worauf sollte bei Therapiebeginn geachtet werden?
Weil Ozanimod das Immunsystem hemmt, sollten vor Therapiebeginn alle Standardimpfungen durchgeführt werden, die die STIKO (Ständige Impfkommission) für Menschen empfiehlt, deren Immunsystem teilweise blockiert werden soll. Insbesondere muss überprüft werden, ob eine Immunität gegenüber Windpocken (medizinisch: Varizellen) besteht – ist dies nicht der Fall, muss unbedingt vor Gabe von Ozanimod gegen Varizellen geimpft werden.
Bei Patienten, die bereits eine Therapie erhalten haben, die das Immunsystem beeinflusst oder hemmt, müssen Sicherheitsabstände vor Umstellung auf Ozanimod eingehalten werden. Diese richten sich nach der Wirkdauer der Medikamente.
Die Wartezeit beträgt nach der Behandlung mit...
- Teriflunomid (nach Auswaschung!) mindestens 4 Wochen.
- Natalizumab mindestens 6-8 Wochen.
- Azathioprin, Ciclosporin A, Cyclophosphamid, Methotrexat und Mitoxantron mindestens 3 Monate.
- Cladribin mindestens 6 Monate.
- Alemtuzumab, Ocrelizumab und Rituximab mindestens 6-12 Monate.
- Bei Interferonen, Glatirameracetat oder Dimethylfumarat müssen, sobald sich etwaige Blutbildveränderungen normalisiert haben, keine Sicherheitsabstände eingehalten werden.
Wann sollte Ozanimod nicht eingenommen werden?
Ozanimod sollte nicht eingenommen werden bei
- einem eingeschränkten Immunsystem
- bestimmten Herz- und Gefäßerkrankungen (bspw. Herzinfarkt, Schlaganfall, vorübergehende Durchblutungsstörungen des Gehirns, einer Herzschwäche innerhalb der letzten 6 Monate)
- schweren Herzrhythmusstörungen (Ausnahme: der Patient verfügt über einen funktionsfähigen Herzschrittmacher)
- aktiven schweren Infektionen (insbesondere Tuberkulose und Hepatitis B und C).
- aktiven Tumorerkrankungen
- deutlichen Leberfunktionsstörungen
- einem Makulaödem (eine Erkrankung des Augenhintergrunds).
- vorliegender Schwangerschaft oder stillenden Patientinnen.
Bei Patienten mit schwerer Atemwegserkrankung, Lungenfibrose oder chronisch-obstruktiver Lungenerkrankung sollte Ozanimod nur mit Vorsicht und nach Absprache mit dem behandelnden Lungenfacharzt angewendet werden. Dies ist darin begründet, dass bei der Behandlung mit Ozanimod geringfügige dosisabhängige Verringerungen der Lungenfunktion beobachtet wurden.
Was muss bei der Behandlung mit Ozanimod kontrolliert werden?
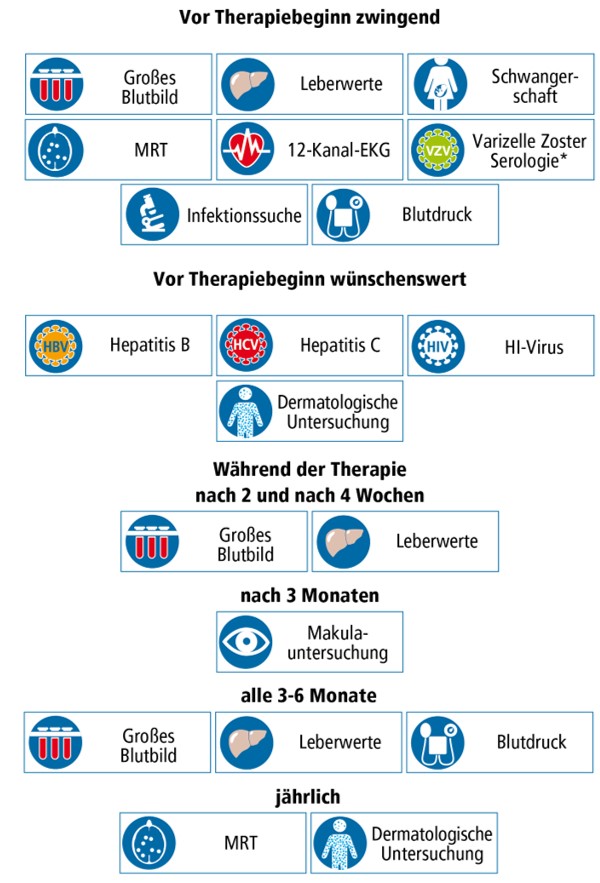
Verminderung der Lymphozyten
Bei Lymphozytenwerten <200 Zellen/µl Blut sollte das Medikament ausgesetzt werden und anschließend alle 2 Wochen Blutbildkontrollen erfolgen. Das Medikament kann erst wieder eingenommen werden, wenn die Lymphozyten mindestens 500/µl betragen.
Wenn die 2-4-wöchigen Blutbildkontrollen initial unauffällig waren, können sie alle 3-6 Monate erfolgen. Wird aber ein Abfall der Lymphozytenzahlen beobachtet, muss wieder engmaschiger kontrolliert werden.
Diese Empfehlungen sind als Vorsichtsmaßnahme zu werten. Gegenwärtig gibt es keinen Anhalt dafür, dass vorübergehende Erniedrigungen der Anzahl von Leukozyten und Lymphozyten ein Risiko darstellen. Bei einer schweren Infektion ist abzuwägen, die Ozanimod-Therapie zu unterbrechen.
Leberwerterhöhungen
Sollten die Leberwerte stark ansteigen (mind. 5-fach über Normalwert), müssen wöchentliche Kontrollen der Werte GOT, GPT, GGT, AP und Bilirubin durchgeführt werden. Bei einem wiederholten Anstieg über das 5-Fache der Normalwerte sollte Ozanimod abgesetzt werden.
Makulaödem
Bei Patienten mit Diabetes mellitus, Entzündungen am Augenhintergrund (einer so genannten Uveitis) oder Vorerkrankungen der Netzhaut sollte eine augenärztliche Untersuchung vor Therapiebeginn mit Ozanimod stattfinden. Während der Therapie mit Ozanimod sollte nach drei Monaten eine Kontrolluntersuchung der Makula durchgeführt werden. Wobald Sehstörungen auftreten, sollte dies in jedem Fall eine Augenuntersuchung stattfinden. Bei Bestätigung eines Makulaödems ist die Therapie mit Ozanimod abzusetzen.
Vor Beginn der Therapie mit Ozanimod und im Verlauf nach 6 Monaten wird eine hautärztliche Untersuchung empfohlen.
Wie lange wird Ozanimod als Therapie eingesetzt?
Empfehlungen für die Tehrapiedauer gibt es bisher nicht. Die Zulassungsstudie RADIANCE untersuchte Ozanimod über den Zeitraum von 2 Jahren, SUNBEAM über 1 Jahr.
Nutzen und Risiko der Einnahme müssen stetig überprüft werden. Ein Abschätzen des Nutzens ist oft frühestens nach einem Jahr möglich. Als Hinweise für eine Wirksamkeit werden allgemeine Schubfreiheit und das Fehlen neuer Herde im MRT angesehen. Deshalb ist eine Ausgangs-MRT und anschließend jährlich eine MRT, um Nutzen und auch mögliche Risiken abzuschätzen.
Häufig gestellte Fragen
Ozanimod sollte in Schwangerschaft und Stillzeit nicht eingenommen werden.
Auf eine wirksame Verhütung sollte geachtet werden. Da Ozanimod über den Einnahmezeitraum hinaus wirken kann, sollte es mindestens 3 Monate vor einem geplanten Schwangerschaftsbeginn abgesetzt werden. Sollte eine ungeplante Schwangerschaft auftreten, muss diese nicht abgebrochen werden, aber Ozanimod sollte sofort abgesetzt werden.
In tierexperimentellen Studien wurde eine schädigende Wirkung von Ozanimod auf den Embryo beobachtet. Es gab ein gehäuftes Auftreten von Fehlgeburten und Herzfehlern. Zur Anwendung von Ozanimod bei schwangeren Frauen gibt es bisher noch keine Erfahrungen.
Möglicherweise geht Ozanimod in die Muttermilch über und sollte in der Stillzeit deshalb nicht eingenommen werden.
Was muss ich bezüglich Impfungen während der Behandlung mit Ozanimod beachten?
Die Wirksamkeit von Impfungen kann während der Einnahme und bis zu 2 Monate nach Absetzen von Ozanimod eingeschränkt sein.
Grippe- und Tetanusimpfungen sind unter Ozanimod wahrscheinlich möglich und wirksam. Sogenannte Lebendimpfstoffe, bei denen lebende, aber abgeschwächte Erreger verwendet werden, sollten möglichst vermieden werden. Ozanimod-Patienten haben möglicherweise keine ausreichende Abwehr und könnten durch die eigentlich harmlosen Impferreger krank werden.
Wie verhalte ich mich bei Infektionen?
Beim Auftreten von Infektionen, vor allem bei anhaltendem oder hohem Fieber, sollte ein Arzt aufgesucht werden. Eine Erregersuche kann begonnen und eine passende Therapie ausgewählt werden. Grundsätzlich muss Ozanimod beim Auftreten üblicher Infekte nicht abgesetzt werden. Bei schweren oder gehäuften Infekten kann im Einzelfall jedoch gemeinsam mit dem Arzt ein Absetzen erwogen werden.
Was geschieht, wenn ich Ozanimod absetze?
Mehrere Fallberichte haben bei dem vergleichbaren Medikament, Fingolimod gezeigt, dass 4 bis 16 Wochen nach Absetzen des Medikaments ein so genanntes Rebound-Phänomen auftreten kann. Dabei kommt es durch den plötzlichen Wegfall der Hemmung durch das Medikament zu einem verstärkten Einstrom von Entzündungszellen ins Nervensystem. Dieses Phänomen kann mit erheblicher Krankheitsaktivität einhergehen. Es ist prinzipiell möglich, dass vergleichbare Effekte nach Therapie mit Ozanimod auftreten.
Gibt es Alternativen zu Ozanimod?
Ozanimod ist nur eine von verschiedenen sicherzugelassenen MS-Therapien. Eine weitere Möglichkeit ist, abzuwarten und (noch) keine Immuntherapie durchzuführen.
Ohne Therapie folgt die MS dem natürlichen Verlauf. Wie dieser über 2 Jahre aussieht, kann man aus Studien ableiten, die ein Medikament mit einem Placebo verglichen haben. Ein Beispiel sind hier Zulassungsstudien des Medikamentes Fingolimod von 2011. Über 2 Jahre blieben in der Placebo-Gruppe 49 von 100 Patienten schubfrei und 82 von 100 (nach 6 Monaten) ohne Zunahme der Behinderung.
Der Vergleich von Ozanimod zu anderen Medikamenten fand in den Studien RADIANCE und SUNBEAM statt, in der es mit Interferon-beta 1a verglichen wurde. Hier zeigte Ozanimod eine Überlegenheit bezogen auf die Schubaktivität, nicht jedoch auch die Zunahme der Beeinträchtigung in der Studienzeit.
Alles auf einen Blick