Interferon-beta (Avonex®, Betaferon®, Rebif®)
Interferone-beta Präparate sind seit 1995 zugelassen. Alle Präparate müssen gespritzt werden, in den Muskel oder unter die Haut. Bei einem Teil der Patienten reduzieren Interferon-beta-Präparate die Schubrate und halten die Zunahme der Behinderung auf. An wichtigen Nebenwirkungen treten auf: grippeähnliche Beschwerden und Reaktionen an den Einstichstellen. Zur Überwachung müssen Laborkontrollen gemacht werden. Inteferon-beta-Präparate werden in der Apotheke unter den Namen Avonex®, Betaferon®, Extavia®, Plegridy® und Rebif® vertrieben.
Wirkungen & Nebenwirkungen im grafischen Überblick
Schubfreie Patienten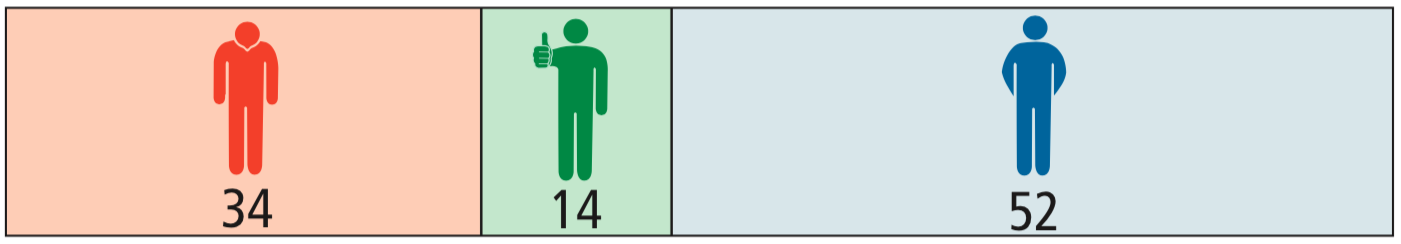

Patienten ohne Zunahme der Behinderung
Es liegen keine aussagekräftigen Studiendaten vor, die einen Effekt von Interferon-beta auf die Behinderungszunahme zeigen.
Wirkung auf MRT-Läsionen
Die Wirksamekit der Beta-Interferoneinnahme kann darüberhinaus bildlich beobachtet werden. Mittels eines MRT (Kernspin) werden für MS typische Entzündungen, die sich als Kontrastmittelanreicherungen und sogenannten T2-Herden zeigen, abgebildet. Diese können nach der Erstmanifestation neu auftreten oder an Größe zunehmen.
Studien vergleichen den zweijährigen Verlauf nach der Erstmanifestation unter der Therapie mit Beta-Interferonen und unter der Einnahme eines Placebos. Gezeigt wurde, dass unter Beta-Interferonen weniger neue Läsionen entstehen.
Die ETOMS-Studie (2001, 309 Patienten) beziffert diesen Effekt: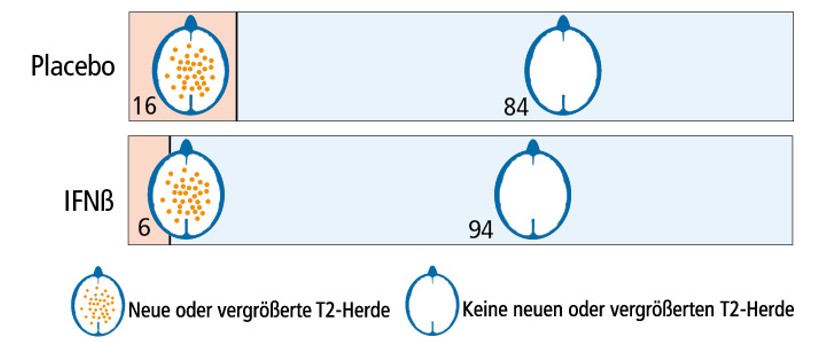
Bezogen auf 100 Patienten zeigen unter der Therapie 6 Patienten, unter Einnahme eines Placebos 16 Patienten neue oder vergrößerte Entzündungen.
Nebenwirkungen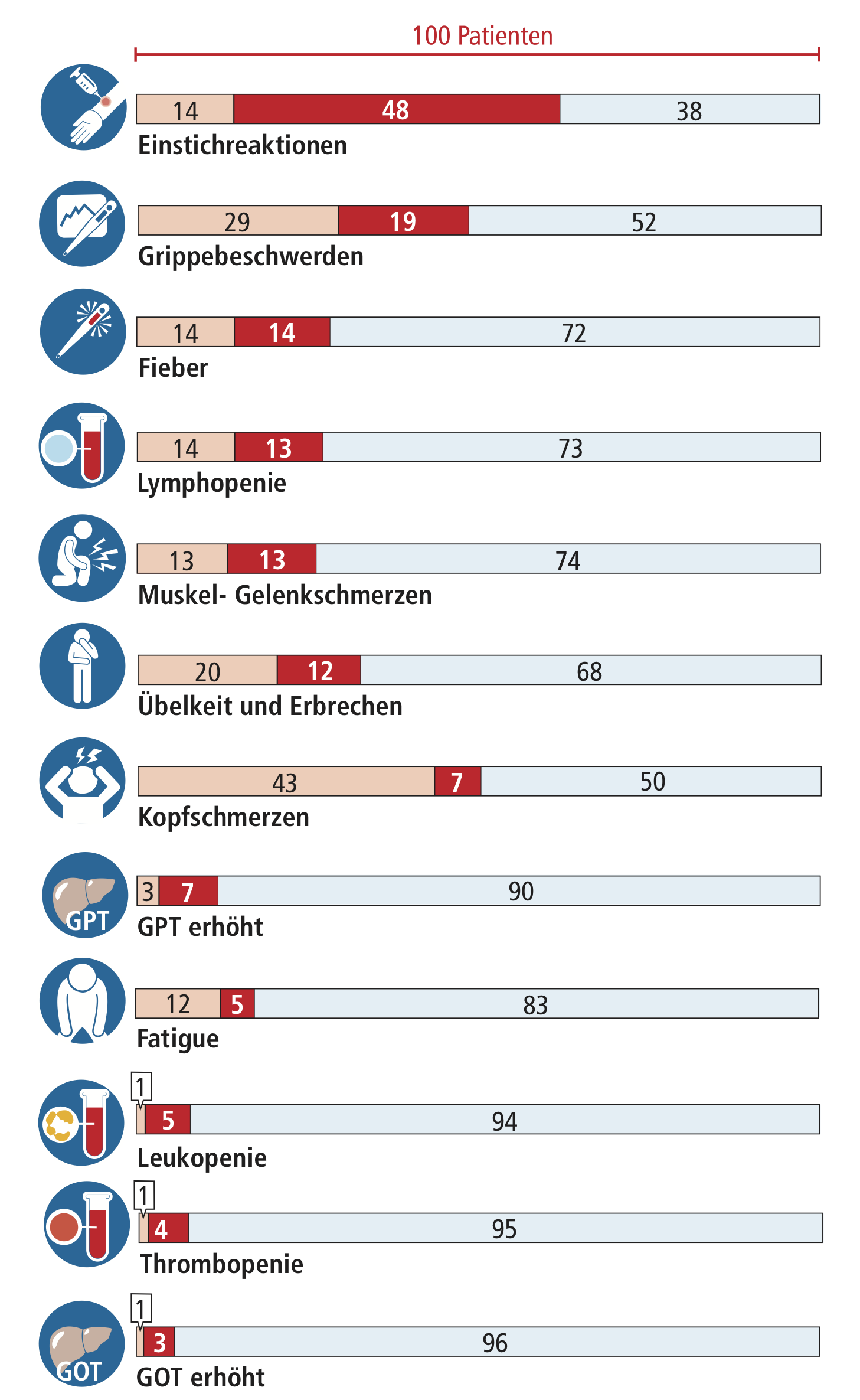
Beta-Interferon (z.B. Avonex®, Betaferon®, Rebif®)
Interferone-beta Präparate sind seit 1995 zugelassen. Alle Präparate müssen gespritzt werden, in den Muskel oder unter die Haut. Bei einem Teil der Patienten reduzieren Interferon-beta-Präparate die Schubrate und halten die Zunahme der Behinderung auf. An wichtigen Nebenwirkungen treten auf: grippeähnliche Beschwerden und Reaktionen an den Einstichstellen. Zur Überwachung müssen Laborkontrollen gemacht werden. Inteferon-beta-Präparate werden in der Apotheke unter den Namen Avonex®, Betaferon®, Extavia®, Plegridy® und Rebif® vertrieben.
Studien
Zur Frage, ob eine ganz frühe Interferontherapie bereits nach dem ersten Schub die Entwicklung einer MS verzögern kann, wurden drei Studien durchgeführt:
- CHAMPS[1] (= Controlled High-risk subjects Avonex Multiple Sclerosis Prevention Study),
- ETOMS[2] (= Effect of early interferon Treatment On conversion to definite Multiple Sclerosis: a randomised study; Rebif®),
- BENEFIT[3] (= Betaferon in newly emerging multiple sclerosis for initial treatment).
Insgesamt wurden 1159 Patienten mit Rebif®, Avonex® oder Betaferon® behandelt. Endpunkt war dabei das Hinausschieben eines zweiten Schubs. Die Studien hatten zum Ziel, die Entwicklung einer gesicherten MS nach den Poser-Kriterien aufzuhalten. In allen drei Studien wurden Patienten mit erstmaligen MS-typischen Beschwerden behandelt, die auch entzündliche Veränderungen im Kernspinbild hatten. Beide Studien unterschieden sich allerdings in den Einschlusskriterien. Die Patienten der Rebif®-Studie und der Betaferon®-Studie hatten mehr Entzündungsherde im Kernspinbild. Die Patienten der Avonex®- Studie erhielten zu Beginn eine Kortisontherapie und wurden früher behandelt. Die Studien sind also nur begrenzt vergleichbar.
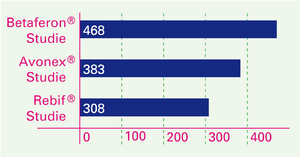
Wirkungen
Zur Therapie der Erstmanifestation sind Betaferon®, Avonex®, Rebif® und Extavia® zugelassen. In den Therapiestudien zu Betaferon® und Rebif® haben 16 von 100 Patienten nach Erstmanifestation innerhalb von 2 Jahren keinen zweiten Schub bekommen. Ob die Frühtherapie grundsätzlich den Verlauf der MS verändert, ist offen.
Anzahl der Patienten mit einem zweiten Schub innerhalb von zwei Jahren
Die Beantwortung der Frage, ob ein zweiter Schub verhindert werden kann, hat bei der Erstmanifestation eine besondere Bedeutung, weil nach der „alten Definition“ (siehe Diagnosekriterien) mit dem Auftreten des zweiten Schubs die Diagnose der MS als gesichert galt.
Der Effekt zeigt sich, wenn man die Anzahl der Patienten mit einem zweiten Schub in der Interferongruppe von denen in der Placebogruppe abzieht. In diesem Falle sind es also 42-26 = 16 von 100 Patienten, die von der Therapie profitieren.
Wirksamkeit auf die Zunahme der Beeinträchtigung in zwei Jahren
Nur in der ETOMS-Studie wurde die Beeinträchtigung mittels EDSS berichtet. Der durchschnittliche EDSS-Wert aller Teilnehmer änderte sich über zwei Jahre nicht. Allerdings hatte ein größerer Prozentsatz (20%) der Nicht-Behandelten eine bestätigte Verschlechterung im EDSS im Vergleich zu den behandelten Patienten (15%). Dieser Unterschied war jedoch nicht signifikant.
Schubrate und Schubschwere
Zum Effekt auf die Schubrate und Schubschwere finden sich in den Veröffentlichungen der Studien keine Informationen.
Im Kernspin feststellbare Wirkung
Die Anzahl von „Kontrastmittel-speichernden Herden“ im Kernspinbild war bei Interferon-behandelten Patienten geringer als in der Placebogruppe. Dies galt auch für die Anzahl neuer Herde. Schließlich zeigte sich, dass Herdgröße bei den Patienten, die Interferon erhielten, deutlich weniger zunahm, als bei Patienten in der Placebogruppe.
Wirkung von Interferonen auf ein Hinauszögern des zweiten Schubs
Bei der Erstmanifestation wurde zusätzlich die Zeitspanne bis zu einem zweiten Schub erfasst. Durch die Interferontherapie ließ sich die Zeit bis zu einem zweiten Schub in der Rebif®-Studie um neun Monate und in der Avonex®-Studie um 13 Monate hinauszögern. Für die Betaferon-Studie liegen diese Zahlen nicht vor. Fasst man diese Ergebnisse zusammen, lässt sich der zweite Schub mit Interferon um durchschnittlich 11 Monate im Vergleich zu Placebo hinauszögern.
Nebenwirkungen
24 von 100 Patienten haben therapiebedingte, grippeähnliche Nebenwirkungen. 48 von 100 Patienten unter einer Rebif®- oder Betaferon®-Therapie haben therapiebedingt Einstichreaktionen. In der Avonex®-Studie gab es eine erhöhte Rate von Depressionen bei den Interferon-behandelten Patienten.
Grippeähnliche Symptome
Bei den mit einem der Interferone behandelten Teilnehmern traten häufiger grippeähnliche Symptome auf als bei den mit Placebo behandelten. In der Interferongruppe hatten 43 von 100 Patienten grippeähnliche Symptome. Darunter fallen auch alle "natürlichen" grippalen Beschwerden wegen eines Virusinfektes, deshalb kann nicht genau gesagt werden, welche grippalen Beschwerden lediglich auf dem Placeboeffekt beruhten. Es haben also mindestens 24 von 100 Patienten therapiebedingt grippeähnliche Nebenwirkungen, maximal 43 Patienten.
Hautreaktionen an der Einstichstelle
Bei der Therapie mit Rebif® und Betaferon® fanden sich oft Hautreaktionen an der Einstichstelle. Aber auch bei den mit Placebo behandelten Patienten traten Hautreizungen an der Einstichstelle auf, so dass dies nicht ausschließlich als Nebenwirkung der Interferongabe gewertet werden kann. In der Rebif®- und Betaferon® Studie hatten 52 von 100 Behandelten und 10 von 100 Placebo- Behandelten solche Nebenwirkungen. 42% der Reaktionen sind somit durch das Interferon verursacht.
Depressionen
Auffallend war in der Avonex®-Studie das häufigere Auftreten von Depressionen in der Behandlungsgruppe: 20 von 100 mit Interferon Behandelten gegenüber 13 von 100 mit Placebo Behandelten erlitten eine Depression. Daraus folgt: 7 von 100 Patienten hatten therapiebedingt eine depressive Verstimmung. Allerdings fanden sich unter Rebif® und Betaferon® keine gehäuften Depressionen, so dass die Bedeutung des Ergebnisses unter Avonex® nicht klar ist.
Schwere Nebenwirkungen
In der Rebif®-Studie wurden in der Behandlungsgruppe sechs und in der Placebogruppe fünf „schwerwiegende Ereignisse“ dokumentiert. In der Avonex®-Studie wird bei einem Patienten unter Avonex®-Therapie und bei sieben Patienten unter Placebo ein solches Ereignis benannt. Dabei wird in beiden Studienberichten nicht genauer erklärt, ob ein Zusammenhang zu den Medikamenten bestand. In der Betaferon®-Studie hatten 20 Patienten unter Betaferon® und 11 Patienten unter Placebo ein schwerwiegendes Ereignis. Hier wird ein Leberwertanstieg als häufigste Ursache genannt.
Andere Nebenwirkungen
Über andere Nebenwirkungen wird in den Veröffentlichungen nicht berichtet.
Schwächen der Interferonstudien zur Erstmanifestation
Der Haupt-Endpunkt der beiden vorliegenden Studien war die Zeit bis zum Auftreten eines zweiten Schubs. Bei der Behandlung von Patienten mit einer Erstmanifestation der MS liegt das Hauptaugenmerk jedoch vielmehr auf der Frage, ob der Krankheitsverlauf durch eine solche Therapie grundsätzlich verändert werden kann und damit das Fortschreiten der krankheitsbedingten Beeinträchtigungen verlangsamt werden kann. Hierüber kann aber anhand der vorliegenden Studienergebnisse allenfalls spekuliert werden.
Langzeitdaten
In der CHAMPIONS-Studie[4] (= Controlled High risk Avonex Multiple Sclerosis Prevention study in ongoing neurological Surveillance) wurden 53% der Patienten der CHAMPS-Studie drei Jahre weiterverfolgt, wobei die Placebogruppe dann auch Avonex® erhielt. Nach fünf Jahren wurde verglichen, wie viele der Patienten mit früher Avonex®-Therapie gegenüber verzögerter Gabe nach zwei Jahren eine sichere MS entwickeln und ob es einen Unterschied in der Beeinträchtigung gibt. Hier fanden sich bei den früh Behandelten 13% weniger sichere MS-Diagnosen nach fünf Jahren. In der Beeinträchtigung zeigten 11% einen EDSS >3 gegenüber 14% der verzögert behandelten Patienten. Eine ähnliche Analyse wurde für 83% der BENEFIT-Studienpatienten[5] nach drei Jahren unternommen. Hier wurde der Effekt einer sofortigen Therapie gegenüber einem um ein Jahr verzögerten Beginn nach fünf Jahren analysiert. 14 von 100 Patienten unter der Frühtherapie hatten einen Nutzen bezogen auf das Verhindern eines zweiten Schubes. 4 von 100 hatten therapiebedingt keine Beeinträchtigungszunahme im EDSS.[5]
Häufig gestellte Fragen
Welches Interferon hilft besser bei der Frühtherapie?
Es gibt keinen direkten Vergleich der Frühtherapeutika Avonex®, Rebif®, Extavia® und Betaferon®.
Welche Nebenwirkungen haben Interferon-beta-Präparate?
Die Gesamtzahl an Nebenwirkungen wird in den Zulassungsstudien meist nicht berichtet. Je älter die Studien, desto uneinheitlicher die Dokumentation. Deshalb lassen sich die Daten zur schubförmigen MS hier auch nicht zusammenfassen. Zur sekundär chronischen MS lässt sich für 5 Zulassungsstudien mit 3082 Patienten zusammenfassen, dass schwere Nebenwirkungen mit 12% in den Interferon-beta-Gruppen genauso häufig auftraten wie unter Placebo. Therapieabbrüche wegen Nebenwirkungen fanden sich mit 10% signifikant häufiger mit Interferon-beta als mit Placebo (4%). Zur Übersichtlichkeit sind im Folgenden die Nebenwirkungen aus den Zulassungsstudien zur schubförmigen MS zusammengefasst. Diese sind bei den KIS-Studien und bei der sekundär chronischen MS ähnlich. Mögliche Unterschiede werden im Text erwähnt.
Grundsätzlich ist wichtig zu wissen, dass Nebenwirkungen in Studien nicht nur bei den Patienten auftreten, die ein neues Medikament erhalten, sondern auch in der Studiengruppe mit einem bekannten Medikament oder Placebo (siehe "Allgemeines zu Wirkungen und Nebenwirkungen von MS-Medikamenten").
Häufige Nebenwirkungen
In der Tabelle sind Nebenwirkungen aufgeführt, die aus der Cochrane Analyse (Rice 2001[1]) berichtet wurden und bei mindestens 2% der Patienten auftraten. Angegeben ist die Patientenzahl von 100 Patienten.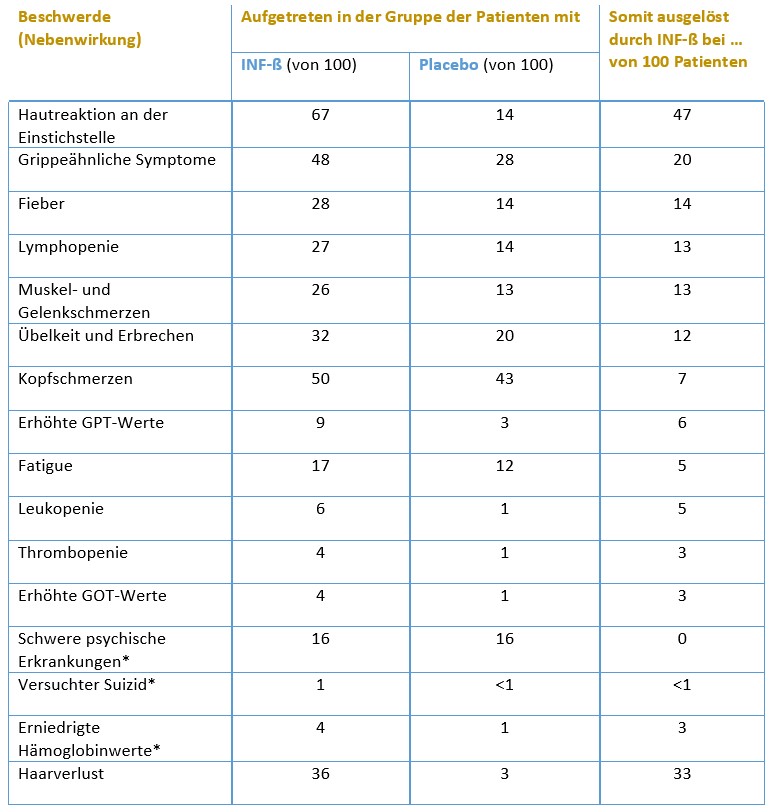
*Bei diesen Nebenwirkungen war der Unterschied zwischen der Interferon-beta- und der Placebo-Gruppe nicht statistisch signifikant.
(Bedingt durch das Runden der Zahlen können kleine Unterschiede (1 von 100) zwischen der Tabelle und der am Kapitelanfang gezeigten Grafik entstehen.)
Reaktionen an der Einstichstelle
Bei der Therapie mit Interferon-beta treten Einstichreaktionen bei subkutaner Gabe mit Betaferon®, Extavia®, Rebif®, Plegridy® sehr häufig auf (zu 50% therapiebedingt). Diese bestehen aus Rötungen und können wochenlang anhalten. Bei intramuskulärerer Gabe werden diese nicht berichtet. Selten kommt es zu schmerzhaften Schwellungen. In manchen Fällen geht das Auftreten von Einstichreaktionen nach und nach zurück. Von offenen Wunden oder auch Nekrosen werden in den Studien bei 2-6% berichtet[100]. Diese heilen wieder ab, bilden dann aber Narben. Bei langandauernder Interferontherapie können auch ohne Nekrosen Vernarbungen oder Verhärtungen im Unterhautfettgewebe entstehen.
Grippeähnliche Beschwerden (Fieber, Kopfschmerz, Muskelschmerz, Fatigue)
Fast die Hälfte der Patienten (48%), die mit Interferon-beta behandelt wurden, hatte Grippesymptome. Aber auch fast 30% der Placebo-Patienten zeigten solche Symptome. Die Beschwerden setzen meist drei bis acht Stunden nach Medikamentengabe ein und halten bis zu 24 Stunden ein. Dabei können auftreten: Fieber, Schüttelfrost, Muskel- oder Gelenkschmerzen, Kopfschmerzen, Abgeschlagenheit und Müdigkeit.
Die Beschwerden können im Verlauf der Therapie abklingen, dann aber im Verlauf wieder erneut auftreten. Bei der Betaferon®-Zulassungsstudie hatten nach einem Jahr noch 8%, bei Rebif® je nach Dosierung 5% bzw. 21% diese Nebenwirkungen. Auch wenn grippe-ähnliche Nebenwirkungen im zweiten Therapiejahr seltener berichtetet werden, so finden sich auch nach 16 Jahren mit Betaferon Therapie bei 1/3 noch berichtete grippeähnliche Beschwerden.
Einige Patienten haben den Eindruck, dass sich die Krankheit unter Einnahme des Interferons verschlechtert, da bedingt durch Nebenwirkungen Müdigkeit und Spastiken verstärkt werden können. Um grippeähnliche Nebenwirkungen zu vermindern, kann vier Stunden vor und evtl. erneut vier Stunden nach Medikamentengabe ein entzündungshemmendes Schmerzmittel (z.B. Paracetamol oder Ibuprofen) eingenommen werden. Sinnvollerweise wird das Interferon abends vor der Schlafenszeit gespritzt, um die Nebenwirkungen weitgehend unbemerkt „auszuschlafen“. Um die Nebenwirkungen von Beginn an gering zu halten, sollte einschleichend behandelt werden, das heißt, die Therapie sollte mit der halben oder evtl. sogar einem Viertel der Injektionsdosis begonnen werden.
Eine kontrollierte Studie[101] mit 160 Patienten konnte zeigen, dass Paracetamol und Ibuprofen gleichermaßen diese Nebenwirkung lindern. Eine andere Studie[33] verglich den Nutzen von Aspirin, Ibuprofen und einer vierwöchigen niedrigdosierten Kortison-Therapie bei 84 Patienten. Auch wenn insgesamt grippeähnliche Nebenwirkungen bei allen gleich häufig und gleich schwer auftraten, so zeigte die Gruppe mit Ibuprofen-Therapie am Tag der Injektion weniger Beschwerden.
Übelkeit und Erbrechen
Übelkeit und Erbrechen treten etwas häufiger unter Interferon-beta auf[1].
Haarausfall
Verstärkter Haarausfall wurde in zwei kleinen Studien mit insgesamt 82 Patienten bei 15 Patienten unter Interferon-beta und nur einer Person unter Placebo berichtet.
Leukopenie, Lymphopenie, Thrombopenie
Bei 5 von 100 Patienten entwickelte sich durch die Interferon-Therapie eine Reduktion der Anzahl an weißen Blutzellen (sogenannte Leukopenie). In Einzelfällen können diese weißen Blutzellen unter 3.000/Mikroliter fallen (Normalbereich: 3.800-10.500/μl). Nur selten können Verminderungen der Blutplättchen, die gemeinsam mit anderen Akteuren für die Blutgerinnung zuständig sind (eine sogenannte Thrombopenie), auftreten. Bislang sind aber noch keine Fälle bekannt, bei denen diese Veränderungen zu ernsthaften Komplikationen geführt haben.
Leberwerterhöhungen
Leberwerterhöhungen unter der Therapie mit ß-Interferon sind häufig.
GPT (heute ALT, nur in der Leber vorkommend) und GOT (heute AST, neben Leber auch in Herz, roten Blutzellen und Muskel vorhanden) sind Enzyme des Aminosäurestoffwechsels in der Leber. Bei einer Leberzellschädigung werden sie in das Blut freigesetzt und können labortechnisch festgestellt werden.
In einer Übersichtsarbeit wurden zur Leberwerterhöhung Daten von 2819 Patienten unter Interferon-beta-1A ausgewertet. Innerhalb von zwei Jahren entwickelten 67% der Patienten im Blut nachweisbare Leberwerterhöhungen, ohne jedoch dahingehende Beschwerden zu haben. Bei 15-20% sind diese Werte bis zu 5-fach über den Normalwert gestiegen, dem gegenüber bei 5% der Placebo-Patienten. Die Laborwerte normalisierten sich wieder, zum Teil nach vorübergehender Dosisreduktion. Nur bei 4 von 1.000 Patienten wurde die Therapie aufgrund der Leberwerterhöhungen abgebrochen. Dieses Risiko scheint im ersten Jahr der Therapie am höchsten. Das Risiko ist erhöht, wenn zusätzlich Alkohol konsumiert wird, Patienten fettleibig sind oder andere Medikamente genommen werden, die die Leberfunktion beanspruchen. Empfehlungen von Experten gehen dahin, bei Erhöhungen um mehr als das 20-fache des Normalwerts die Therapie vorübergehend auszusetzen. Bislang wurde nur in Einzelfällen von schweren Leberschädigungen unter Beta-Interferon berichtet.
Schwere Nebenwirkungen und Todesfälle
Durch Interferon-beta bedingte schwere Nebenwirkungen und Todesfälle traten in den Studien nicht gehäuft auf. In einer der KIS-Studien[102] kam es in der Interferon-Gruppe zu einem Toten durch einen Autounfall. In den Studien zur schubförmigen MS kam es unter Betaferon zu einem Selbstmord, in der Rebif-Studie zur schubförmigen MS (PRISMS[6]) kam es zu je einem Todesfall unter Placebo und einem unter 22ug Rebif. Bei den SPMS-Studien traten Todesfälle laut einer Metaanalyse[103] etwas häufiger mit Interferon-beta auf. Unter Interferon-beta kam es zu 17 Todesfällen, 4 durch Selbstmord, 3 Lungenembolien, 3 Herzstillstände, 1 Krebserkrankung, eine Blutung im Kopf, 2 Schlaganfälle und eine schwere Harnwegsinfektion; bei 2 Fällen blieb die Ursache unklar. In den Kontrollgruppen kam es insgesamt zu 7 Todesfällen: 2 Selbstmorde, eine Blutung im Kopf, eine Gefäßerkrankung (Arteriosklerose), eine Lungenentzündung, 2 unbekannte Todesursachen.
In der Fachliteratur sind Einzelfälle schwerer Nebenwirkungen beschrieben, bei denen ein Zusammenhang folgender Beschwerden mit der Interferon-Gabe für wahrscheinlich gehalten wird: Blutarmut, Überaktivität der Schilddrüse, Nierenfunktionsausfall, Verstopfung von kleinen Blutgefäßen, allergischer Schock und epileptische Anfälle. Weiter finden sich vereinzelt Entzündungen im Fettgewebe der Haut und andere Hautveränderungen sowie Leberentzündungen und Muskelschädigungen.
Krebserkrankungen
In den Studien wird nur bei der SPMS eine Krebserkrankung aus einer Interferon-beta-Gruppe beschrieben. Oft fehlt in den Studien jede Aussage zu möglichen Krebserkrankungen. Damit ist eine belastbare Risikoeinschätzung nicht möglich. Es erscheint aber heute, 25 Jahre nach Zulassung der ersten Interferone, mit keinerlei Langzeithinweis auf Krebserkrankungen sehr unwahrscheinlich, dass Interferone Krebserkrankungen hervorrufen.
Infektionen
Infekte traten bei der Therapie mit Interferonen nicht gehäuft auf. Auch die Langzeitstudien sprechen nicht dafür.
Welche neuen Nebenwirkungen wurden nach Abschluss der Zulassungsstudien berichtet?
Einzelfälle von akutem Leberversagen sowie von einer akuten Nierenerkrankung mit Eiweißverlust sind im Verlauf nach Zulassung der Interferon-beta-Präparate beschrieben worden. Weitere besondere Nebenwirkungen sind 25 Jahre nach der ersten Interferon-Zulassung nicht berichtet worden.
Worauf muss bei der Therapie mit Interferon-beta geachtet werden?
Weil Interferon-beta-Präparate das Immunsystem verändern, sollten vor Therapiebeginn alle Standardimpfungen durchgeführt werden, die die STIKO (Ständige Impfkommission) für Menschen empfiehlt, deren Immunsystem teilweise blockiert werden soll.
Bei Patienten, die bereits eine Therapie erhalten haben, die das Immunsystem beeinflusst oder hemmt, müssen Sicherheitsabstände (siehe weiter unten) eingehalten werden. Diese richten sich nach der Wirkdauer der Medikamente. Eine Kurzzeitbehandlung mit Kortikosteroiden (Kortison), z.B. zur Schubtherapie, ist auch während der Behandlung möglich.
Unter welchen Umständen sollten Interferone nicht verabreicht werden?Laut Empfehlungen des Kompetenznetzes MS (KKNMS) sollten Interferon-beta-Präparate nicht eingenommen werden bei:
- Überempfindlichkeit gegen die Substanz oder einen der sonstigen Bestandteile
- Therapiebeginn in der Schwangerschaft
- Schwere akuter Depression oder Suizidalität.
Bei Patienten, die bereits eine Therapie erhalten haben, die das Immunsystem beeinflusst oder hemmt, müssen vor einer Umstellung auf Interferone bestimmte Sicherheitsabstände eingehalten werden. Diese richten sich nach der Wirkdauer der Medikamente. Die Wartezeit beträgt nach der Behandlung mit...
- Fingolimod und Teriflunomid (nach Auswaschung!) mindestens vier Wochen.
- Natalizumab und Daclizumab mindestens sechs bis acht Wochen.
- Azathioprin, Ciclosporin A, Cyclophosphamid, Methotrexat und Mitoxantron mindestens drei Monate.
- Cladribin mindestens 6 Monate.
- Alemtuzumab, Ocrelizumab und Rituximab mindestens 6 – 12 Monate.
Was muss bei der Therapie kontrolliert werden?
Das Krankheitsbezogene Kompetenznetz Multiple Sklerose (KKNMS) empfiehlt:
GRAFIK FOLGT
Interferon-beta - Häufig gestellte Fragen
Bislang liegen vier direkte Vergleichsstudien vor, die aber methodische Mängel hatten und zumeist nur zwei Substanzen miteinander verglichen. Eine nicht systematische Übersicht kommt zu dem Ergebnis, dass es einige Hinweise für eine Überlegenheit höher dosierter Interferon-beta Präparate auf die Reduktion der Schubrate gibt (Freedman 2009). Ein eindeutiger Beleg fehlt jedoch. Intramuskuläre Präparate führen zu weniger Hautreaktionen. Die seltenere Gabe führte zu selteneren Hautreaktionen und grippeähnlichen Beschwerden. Möglicherweise ist jedoch die Intensität der Beschwerden stärker.
Wie lange wird behandelt?
Eine Interferon-Therapie wird als Dauertherapie eingesetzt. Nutzen und Risiko der Einnahme müssen laufend überprüft werden. Ein Abschätzen des Nutzens ist oft frühestens nach einem Jahr möglich. Als Hinweise für eine Wirksamkeit werden allgemeine Schubfreiheit und das Fehlen neuer Herde in der MRT angesehen. Deshalb empfiehlt das KKNMS eine Ausgangs-MRT und eine MRT nach 6, 12 und 24 Monaten, um Nutzen und auch mögliche Risiken abzuschätzen.
Wenn es keinen klinsichen Anhaltspunkt für einen Krankheitsprogress gibt und ein standardisiertes Ausgangs-MRT vorliegt, sollte auf eine Kontrastmittelgabe verzichtet werden.
Schwangerschaft und Stillzeit
Die Interferon-beta Präparate Betaferon® und Rebif® sind seit 2019 in Schwangerschaft und Stillzeit zugelassen. Die in Tierversuchen nachgewiesene erhöhte Fehlgeburtsrate konnte in Fallsammlungen von Patienten, die während der Einnahme eines Interferon-beta Präparates schwanger wurden, nicht bestätigt werden.
Eine Übersicht berichtet von 761 Schwangerschaften, die unter einer Interferon-beta Therapie auftraten ("Disease-modifying drugs for multiple sclerosis in pregnancy: a systematic review"[35]). Hier fanden sich zwar ein erniedrigtes Geburtsgewicht und geringere Größe sowie eine erhöhte Frühgeburtlichkeit, jedoch nicht mehr Aborte oder Missbildungen als bei Schwangerschaften ohne Interferon-Exposition. Insgesamt scheint das Risiko für Schäden eines Embryos sehr gering zu sein. Eine neuere Übersicht ("Pregnancy outcomes in interferon‐beta‐exposed patients with multiple sclerosis: results from the European Interferon‐beta Pregnancy Registry"[96]) konnte bei 945 Schwangerschaften unter Interferon-beta keine Missbildungen oder Frühgeburten zeigen.
Impfungen
Auch unter einer Therapie mit Interferon-beta sollten alle Standardimpfungen regelmäßig überprüft und ggf. aufgefrischt werden. Die Ständige Impfkommission, kurz STIKO, entwickelt Impfempfehlungen für Deutschland, die als medizinischer Standard gelten. Laut der STIKO sind die Standardimpfungen: Tetanus, Diphtherie, Pertussis (Keuchhusten), Hepatitis B, Masern, Mumps, Röteln.
Für alle MS-Patienten ist eine Grippeimpfung sinnvoll. Pneumokokken und Windpocken (Varizella-Zoster-Virus) sind für eine Interferontherapie nicht erforderlich. Mit Blick auf mögliche Therapieeskalationen kann aber auch hier früh eine Impfung erwogen werden.
Bisher gibt es einige Hinweise, dass Impferfolge unter Interferon-Therapie etwas abgeschwächt sind. Einige wenige Daten sprechen dafür, dass Standardimpfungen unter Interferonen wirksam bleiben.
Interferone
Grundsätzlich müssen Interferone beim Auftreten üblicher Infekte nicht abgesetzt werden.
Welche Bedeutung haben sogenannte neutralisierende Antikörper?
Interferone rufen im Körper die Bildung von Antikörpern hervor, da sie nicht genau dem körpereigenen Interferon entsprechen. Antikörper können mit verschiedenen Methoden gemessen werden. Diese Antikörper können möglicherweise die Wirkung des Interferons abschwächen oder ganz verhindern.
Die Antikörper entstehen meistens innerhalb der ersten 12 Monate nach Therapiebeginn. Die Häufigkeit unterscheidet sich bei den Präparaten: Betaferon/Extavia mehr als Rebif, mehr als Avonex, mehr als Plegridy. Ein systematisches Review ("Development of interferon beta-neutralising antibodies in multiple sclerosis"[97]) kommt zu folgenden Raten: 2-19% bei Avonex, 16-35% bei Rebif und 27-53% bei Betaferon. Für Plegridy wurden bislang nur sehr niedrige Raten unter 1% beschrieben. Wichtig ist, dass sowohl die Höhe der Antikörperwerte als auch das länger bestehende Vorliegen hoher Werte eine maßgebliche Rolle für den neutralisierenden Effekt zu spielen scheinen: hohe Werte (hochtitrige), die bleiben.
Eine grundsätzliche Testung nach frühestens vier bis sechs Monaten kann erwogen werden. Da neutralisierende Antikörper kreuzreaktiv sind, ist ein Wechsel von einem Interferon-beta-Präparat auf ein anderes bei Therapieversagen durch die Antikörper-Bildung vermutlich nicht sinnvoll.
Machen Interferone depressiv?
Bei 35-55% aller MS-Patienten treten irgendwann depressive Verstimmungen auf. Ein systematisches Review (Alba Palé L 2017[98]) kommt zu dem Ergebnis, dass nur bei Patienten mit vorbekannter Depression eine Interferon-beta-Therapie zur Depressionsverstärkung führen kann.
Welche Alternativen bestehen zu Interferon-beta-Präparaten?
Interferon-beta ist nur eine von verschiedenen zugelassenen MS-Therapien. Eine Übersicht finden Sie auf der Hauptseite. Eine weitere Möglichkeit ist auch, (noch) keine Immuntherapie durchzuführen.
Ohne Therapie folgt die MS dem natürlichen Verlauf. Wie dieser aussieht, kann man aus den Daten der Placebo-Gruppe in der Zulassungsstudie abschätzen: Über 2 Jahre blieben in der Placebo-Gruppe 70 von 100 Patienten schubfrei und 70 von 100 ohne Zunahme der Behinderung.
Wirken Interferone besser oder schlechter als andere MS-Medikamente?
Die Wirksamkeit von Beta-Interferonen im Vergleich mit Glatirameracetat wurde in 6 Vergleichsstudien analysiert. Eine Metanalyse von 5 dieser Arbeiten (Mantia and Pietrantonj 2014[99]) kommt zu dem Ergebnis, dass die Wirkung sehr vergleichbar ist.
Interferon-beta Präparate haben in mehreren Studien Gleichwertigkeit zu Copaxone® gezeigt. Belastbare Vergleiche mit Teriflunomid und Dimethylfumarat fehlen.
Wann sollte eine Interferon-beta-Therapie abgesetzt werden?
Für die Interferone existieren einige Daten zur Vorhersage, ob die Therapie wirkt oder nicht. Das Kernspin (MRT) ist dafür möglicherweise hilfreich.
Entwickeln Patienten unter der Therapie mit Interferon-beta eine nicht-aktive sekundär progrediente MS, sollte die Tehrapie nciht fortgesetzt werden.
Interferon-beta - Alles auf einen Blick