Wie kann Multiple Sklerose diagnostiziert werden?
Leider gibt es keinen einzelnen diagnostischen Test, der beweisend für MS ist. Auch wenn alle Diagnosekriterien erfüllt sind, kann es sich im späteren Verlauf noch herausstellen, dass es sich doch um eine andere Erkrankung handelt. Die Diagnose beruht auf Entzündungsherden an verschiedenen Stellen und zu verschiedenen Zeiten im Nervensystem und klinischen Beschwerden (Schüben). Seit 2010 ist eine Diagnosestellung bereits nach einem ersten Schub, basierend auf mindestens einer Kernspinuntersuchung, möglich. Nervenwasseruntersuchungen liefern darüber hinaus wichtige Informationen durch den Nachweis so genannter „oligoklonaler Banden“.
Diagnostische Methoden
Erheben der Krankengeschichte (Anamnese)
Wenn Patienten mit neu aufgetretenen neurologischen Symptomen zum Arzt gehen, kommen zunächst eine Vielzahl an Erkrankungen in Frage, vom Schlaganfall über entzündliche oder infektiöse Erkrankungen bis hin zum Tumor. Der Arzt erhebt als erstes die Krankengeschichte des Patienten:
- Welche Symptome beschreibt der Patient,
- wann haben sie begonnen,
- haben sie sich verschlechtert oder bereits wieder verbessert,
- wo sind sie lokalisiert? usw.
Darüber hinaus wird nach Erkrankungen und Operationen in der Vergangenheit gefragt sowie nach Krankheiten bei nahen Familienangehörigen. Auf diese Art und Weise kann der Kreis der Verdachtsdiagnosen bereits eingeengt werden.
Neurologische Untersuchung
Ziel der neurologischen Untersuchung ist es, die vom Patienten beschriebenen Symptome objektiv zu erheben sowie ggf. andere Symptome, die vielleicht noch gar nicht als solche bemerkt wurden, zu erkennen. Die neurologische Untersuchung prüft nacheinander alle neurologischen Funktionssysteme durch: u.a. Gefühl, Motorik, Koordination, Hirnnerven, Reflexe.
Wenn sich aus der Krankengeschichte und der neurologischen Untersuchung der Verdacht auf eine Multiple Sklerose ergibt, werden die Kernspintomographie und die Lumbalpunktion angeschlossen.
Kernspintomographie (Kernspin)
Die Kernspintomographie(auch Magnetresonanztomographie (MRT) oder Kernspintomogramm oder Kernspin gennannt) ist neben der körperlichen Untersuchung das wichtigste diagnostische Hilfsmittel bei MS. Mit der MRT lassen sich die Strukturen des Gehirns relativ gut abbilden. Ein Kernspin dauert ca. 20 Minuten beim Kopf und ca. 30 Min, wenn die gesamte Wirbelsäule dargestellt werden soll.
Bei der MRT werden durch ein starkes Magnetfeld alle Atomkerne im Körper gleich ausgerichtet. Gemessen wird dann nach Ausschaltung des Magnetfeldes, wie die Atomkerne in ihren Grundzustand zurückschwingen. Dieser Prozess kann anschließend auf unterschiedliche Arten analysiert werden, man spricht von MRT-Sequenzen. Welche Sequenzen untersucht werden, hängt von der Fragestellung der Untersuchung ab. Derselbe Gewebetyp kann in verschiedenen Sequenzen völlig unterschiedlich zur Darstellung kommen. Bei der MS-Diagnostik werden andere Sequenzen untersucht als beispielsweise in der Schlaganfall- oder Hirntumordiagnostik.
Das Gehirn ist innen und außen von Nervenwasser (Liquor) umgeben. Die „bananenförmigen“ Gebilde in der Mitte des Kernspinbildes (in Queraufnahme (siehe Abbildung)) sind zwei der inneren Nervenwasserräume, auch Ventrikel genannt. Hier werden der erste und zweite Ventrikel symmetrisch in den Hirnhälften sowie vom dritten Ventrikel in der Mitte darunter und dem vierten Ventrikel zwischen Hirnstamm und Kleinhirn (s.u.) unterschieden. Das Kernspin zeigt beim Gehirn Hirnrinde (auch graue Substanz genannt) und Marklager (auch weiße Substanz genannt). In der Hirnrinde befinden sich die Nervenzellkörper, im Marklager die Nervenzellfortsätze. Im Gehirn werden das Großhirn, das Kleinhirn und der Hirnstamm unterschieden. Das Großhirn macht einen Großteil des Gehirns aus und ist für alle Denkprozesse, Wahrnehmungen und Bewegungen zuständig. Die beiden Hirnhälften verbindet der sogenannte Balken. Er liegt oberhalb der beiden seitlichen Nervenwasserräume. Das Kleinhirn ist wesentlich für die Koordination. Es ist durch ein Dach, das „Tentorium“ nach oben vom Großhirn getrennt. In der Beschreibung von MS-Herden wird oft von „supratentoriellen“ und „infratentoriellen“ Herden gesprochen. Damit sind Entzündungsherde ober- bzw. unterhalb einer gedachten Linie auf der Höhe des Kleinhirndachs gemeint. Der Hirnstamm ist die Verbindung von Großhirn und Kleinhirn zum Rückenmark. Hier werden z.B. wichtige Funktionen der Augenbewegungen, das Sprechen und Schlucken sowie weitere unbewusst ablaufende lebenserhaltende Funktionen (Atmung, Temperaturregulation) koordiniert.
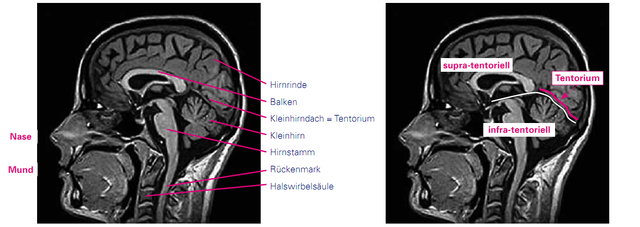
Abb.: Kernspin des Kopfes seitlich (T1-Sequenz)
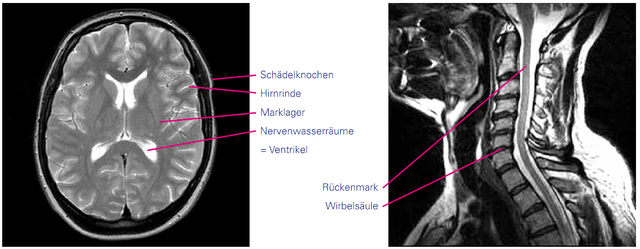
Abb.: Kernspin des Kopfes (T2-Sequenz) (links) und Kernspin des Halses (rechts)
Kernspinaufnahmen mit der T1-Sequenz
Hier erscheint alles grau und schwarz. T1-Sequenzen sind gut geeignet, um bleibende Gewebeschäden zu erkennen. Im Marklager finden sich meist rundliche Flecken. Dabei ist wichtig zu beachten, dass unterschiedliche Graustufen das unterschiedliche Ausmaß der Gewebeschädigung widerspiegeln. Diese Flecken werden „hypointens“ genannt (hypo = unter, niedrig). Auch diese Hypointensitäten bilden sich teilweise wieder zurück. Nur ein kleiner Teil wird zu bleibenden „schwarzen Löchern“ als Ausdruck bleibenden Gewebeschadens. In T1 lässt sich ferner das Schrumpfen des Gehirns über die Zeit, das bei MS-Betroffenen schneller voranschreiten kann als bei Gesunden am besten analysieren.
Kontrastmittel-verstärkte T1-Bilder
Oft erfolgt eine Kontrastmittelgabe über eine Vene im Arm. Das Kontrastmittel, z.B. Gadolineum, gelangt an Stellen in das Gehirn, an denen die Barriere zwischen Blut und Gehirn gestört ist. Dies lässt sich im T1-Bild als weißer Fleck identifizieren. Diese Störungen der so genannten Blut-Hirn-Schranke sind Ausdruck frischer entzündlicher Krankheitsaktivität. Kortison kann diese Störung gut unterdrücken. Deshalb ist eine Kontrastmittelgabe innerhalb der ersten vier Wochen nach einer Kortisontherapie meist nicht sinnvoll.
Kernspinaufnahmen mit der T2- oder FLAIR-Sequenz
Bei diesen Darstellungen können Entzündungsherde am besten entdeckt werden. Diese erscheinen im Bild jeweils hell oder „hyperintens“. Das Nervenwasser erscheint weiß in T2 und schwarz im FLAIR. Da bei MS die Veränderungen oft dicht an den Ventrikeln liegen, ist die FLAIR-Sequenz am besten geeignet, diese Entzündungsherde zu zeigen. Diese Herde können kommen und gehen. Viele sind im Verlauf nicht mehr nachweisbar.
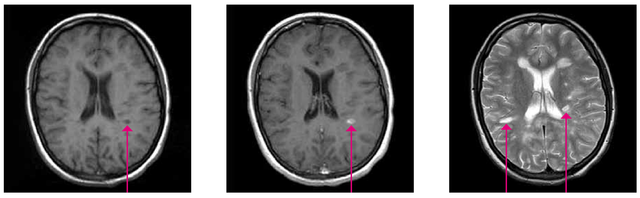
Abb. 14, 15, 16: "Schwarzes Loch" in T1 (links), Kontrastmittelanreicherung in T1 (Mitte), Entzündungsherde in T2 (rechts)
Einschränkungen des Kernspins
Aus der Anzahl an T2- oder FLAIR-Entzündungsherde allein oder deren Größe lässt sich nicht auf die Beeinträchtigung schließen.[1] So gibt es Betroffene, die sehr viele Herde aber keine Beschwerden haben, während es anderen mit wenigen Herden schlecht geht. Wesentlich für die Bedeutung von Kernspinherden ist
- ob sie in einer Region liegen, die empfindlich für das Auftreten von Einschränkungen (z.B. Hirnstamm oder Rückenmark) ist und
- ob nur eine vorübergehende Störung vorliegt oder sich eine bleibende Schädigung, ein so genanntes schwarzes Loch herausbildet.
Auch die Bedeutung des Kernspins für den weiteren Verlauf ist für alle oben genannten Sequenzen gering.[2]
Für die Abschätzung der Prognose der MS-Erkrankung wird das Kernspin ebenfalls genutzt. Um mehr zu erfahren, lesen Sie hier weiter...
Das Nervenwasser (Liquor) umspült das Gehirn von innen und außen und federt es in einer Art Wasserkissen ab. Täglich werden ca. 300 ml neu gebildet. Mit der Nervenwasserraumpunktion (Lumbalpunktion, LP) lässt sich die Zusammensetzung des Nervenwassers untersuchen, hierbei interessieren vor allem Entzündungszellen und Eiweiße.
Die Lumbalpunktion ist eine häufig durchgeführte Maßnahme, die bisweilen mit unangenehmen Nebenwirkungen verbunden sein kann. Sie lässt sich meist ambulant durchführen und dauert ca. 10 Minuten. Mit einer dünnen Nadel wird auf Höhe des Beckens zwischen zwei Wirbelkörpern eine Punktion gemacht und ca. 10-30 ml Nervenwasser abgenommen. Auf dieser Höhe findet sich kein Rückenmark mehr, sondern nur Nervenfäden, die selten einmal von der Punktionsnadel berührt werden können, was zu einer elektrisierenden Missempfindung (ähnlich dem Gefühl beim Berühren eines elektrischen Zauns) führt, aber ohne Folgen bleibt. Die Nerven weichen der Nadel aus und werden nicht aufgespießt.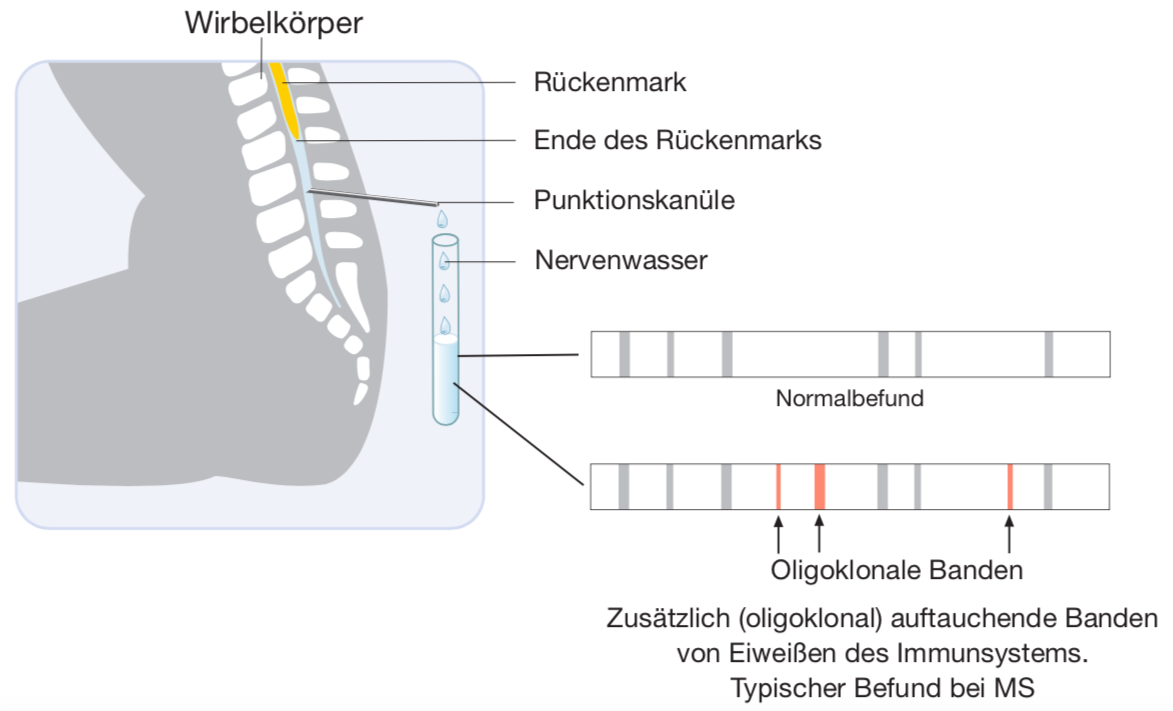
Die häufigste Nebenwirkung bei bis zu 10% der Punktionen mit neuer Nadeltechnik ist das so genannte postpunktionelle Syndrom. Hier entwickeln sich Kopfschmerzen, die typischerweise nur in aufrechter Haltung auftreten und im Liegen verschwinden. Manchmal sind sie von Übelkeit und Erbrechen begleitet. Schlimmstenfalls muss man damit 7-10 Tage weitgehend das Bett hüten. Fast immer verschwinden sie nach dieser Zeit. Ursache ist ein Leck des Liquorraums, das auch nach Entfernung der Nadel für einige Tage bleibt. Damit entsteht ein Unterdruck im Nervenwassersystem und das Gehirn „rutscht“ beim Aufstehen nach unten und zerrt an den Hirnhäuten, was Kopfschmerzen verursacht. Bei ausgeprägten Beschwerden kann man durch einen so genannten Eigenblutpatch 10-20ml Blut an die Punktionsstelle spritzen und so das Leck verkleben. Sehr selten kann es zu Infektionen und Blutungen, kommen.[3]
Liquorbefunde
- Zellen: Normalerweise finden sich im Liquor allenfalls wenige weiße Blutzellen oder „Lymphozyten“. Bei MS ist diese Anzahl leicht vermehrt von fünf Zellen pro Mikroliter (μl) (entsprechend 15 „Drittelzellen“ bei anderer Bestimmungsweise) bis zu ca. 50 Zellen pro μl (150 „Drittelzellen“). Meist sind diese Zellen Lymphozyten. Bei deutlich höherer Zellzahl liegt wahrscheinlich keine MS vor.
- Eiweiß: Alle Eiweißbestandteile des Blutes finden sich auch im Liquor. Der Hauptanteil ist dabei das so genannte Albumin. Blut und Liquoreiweiss stehen in einem bestimmten Mengenverhältnis zueinander. Ist dies gestört, so kann auf eine isolierte Störung im Nervensystem geschlossen werden. Der Gesamtgehalt liegt bei 500 mg pro ml. Bei MS ist dieser Wert nicht verändert, bei deutlich erhöhtem Wert liegt wahrscheinlich keine MS vor.
- Antikörper: Zusätzlich bestimmt man den Gehalt bestimmter Antikörper im Nervenwasser und Blut. Man unterscheidet vier Klassen: Immunglobulin M (IgM) ist ein Frühantikörper bei Infektionen, ihm folgt Immunglobulin G (IgG). Im Speichel findet sich Immunglobulin A (IgA) und bei allergischen Reaktionen ist Immunglobulin E (IgE) beteiligt. Antikörper sind Teil des immunologischen Gedächtnisses und bei allen Menschen vorhanden. Infektionen und Impfungen hinterlassen spezifische Antikörper quasi als Erinnerung. Typischerweise findet man bei MS eine isoliert im Nervensystem nachweisbare Produktion von IgG, seltener auch IgM. Dies lässt sich über den so genannten IgG-Index aus dem Verhältnis der Konzentrationen in Blut und Liquor errechnen und manchmal auch als Menge quantitativ bestimmen. Dieser Index ist beim Gesunden kleiner als 0,7. Gelingt dieser quantitative Nachweis nicht, so kann man mit einer sehr feinen Methode auch eine geringe isolierte Produktion von Antikörpern im Nervensystem nachweisen. Dazu lässt man die Liquoreiweisse auf einer Platte in einem elektrischen Feld wandern, was zu einer Auftrennung nach Größe und elektrischen Eigenschaften führt (genannt: Elektrophorese). Nach dieser Auftrennung erfolgt eine Färbung. Hier können dann so genannte „oligoklonale Banden“ nachweisbar sein. Das sind Antikörper, die von einer kleinen Anzahl (oligo=wenige) von Gruppen von Antikörper-produzierenden Zellen aus einer Ursprungszelle (=Klon) gebildet werden. Diese Antikörper sind als Streifen (oder Banden) in einer Färbung nachweisbar. (siehe Abb. unten) Findet man isoliert im Liquor mehr als drei dieser oligoklonalen Banden so ist der Liquorbefund nach Expertenkonsens als MS-typisch und positiv zu bewerten.

Abb.: Oligokonale Banden sind auf dem Elektrophorese-Gel erkennbar
Unter diesen in den Banden abgebildeten Antikörpern befinden sich sowohl Antikörper gegen bekannte Erreger, wie z.B. Masernviren oder das Epstein-Barr Virus (EBV) aber auch so genannte Auto-Antikörper, die sich beispielsweise gegen Myelin richten. Solche Auto-Antikörper kommen auch bei gesunden Menschen vor, sodass die Bedeutung der oligoklonalen Banden für die Entstehung der MS unklar ist. Sind sie einmal nachweisbar, verschwinden sie auch meist nicht wieder. Wenn sie einen typischen Befund erbracht hat, ist die Lumbalpunktion bei MS nur einmal erforderlich.
Andere mögliche Diagnosen (Differentialdiagnosen)
Eine häufig gestellte Differentialdiagnose ist die Borreliose, also eine per Zeckenbiss übertragene Infektionserkrankung. In der Regel verursacht sie aber eher andere Beschwerden und einen anderen Liquor- und Kernspinbefund. Ausschlaggebend sind typische Hautveränderungen zu Beginn und Antikörper- sowie Borreliennachweistests aus Blut und Liquor.
Andere erregerbedingte Erkrankungen wären z.B. eine Syphilis oder auch eine Mitbeteiligung bei HIV. Gefäßbedingte Erkrankungen, wie kleine Schlaganfälle, evtl. auf Basis einer Gefäßentzündung oder einer anderen Autoimmunerkrankung, die zu Gefäßveränderungen führt (z.B. Lupus erythematodes oder Anti-Phospholipid-Syndrom) sollten ausgeschlossen werden.
Bei einer Rückenmarks- und Sehnervbeteiligung, muss an eine Neuromyelitis optica gedacht werden. Wenn nur das Rückenmark im Vordergrund steht, ist ein Sjögren-Syndrom zu diskutieren wie auch Tumore oder Gefäßmissbildungen im Rückenmark. Andere Autoimmunerkrankungen mit Befall des zentralen Nervensystems und evtl. MS-ähnlichem Bild sind die Neurosarkoidose oder der Morbus Behcet.
Einzelnachweise
- ↑ Goodin DS. Magnetic resonance imaging as a surrogate outcome measure of disability in multiple sclerosis: have we been overly harsh in our assessment? Ann Neurol 2006; 59(4):597-605.
- ↑ Daumer M et al. MRI as an outcome in multiple sclerosis clinical trials. Neurology 2009; 72(8):705-11.
- ↑ Williams J et al. Diagnostic lumbar puncture: minimizing complications. Intern Med J 2008; 38(7):587-91.
- ↑ Poser CM et al. New diagnostic criteria for multiple sclerosis: guidelines for research protocols. Ann Neurol 1983; 13:227-31.
- ↑ McDonald WI et al. Recommended diagnostic criteria for multiple sclerosis: guidelines from the International Panel on the diagnosis of multiple sclerosis. Ann Neurol 2001; 50:121-7.
- ↑ 6,0 6,1 Polman CH et al. Diagnostic Criteria for Multiple Sclerosis: 2010 Revisions to the McDonald Criteria. Ann Neurol 2011; 69:292–302.
- ↑ Deutsche Gesellschaft für Neurologie (DGN)/ Kompetenznetz Multiple Sklerose (KKNMS). Leitlinie zur Diagnose und Therapie der MS. Online-Version. Stand: 12.04.2012. URL: [Homepage der deutschen MS-Gesellschaft]; Zugriff am 12.01.2014.
- ↑ 8,0 8,1 Swanton JK et al. MRI criteria for multiple sclerosis in patients presenting with clinically isolated syndromes: a multicentre retrospective study. Lancet Neurol 2007; 6:677–86.
