Ocrelizumab (Ocrevus®)
Ocrelizumab (Ocrevus®) wird halbjährlich als Infusion über eine Vene (intravenös) verabreicht. Ocrelizumab ist für Patienten mit schubförmiger und aktiver primär progredienter MS zugelassen. Bei einem Teil der Patienten reduziert es die Häufigkeit von Schüben und hält die Zunahme der Behinderung auf. Dass Ocrelizumab so selten verabreicht werden muss, liegt daran, dass das Medikament das Immunsystem langfristig beeinflusst.
Die wichtigsten Nebenwirkungen sind: Infusionsreaktionen und Infektionen.
Patienten ohne Zunahme der Behinderung

Nebenwirkungen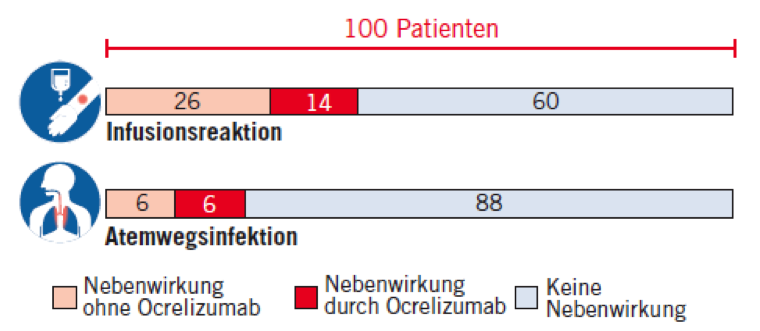
Was ist Ocrelizumab?
Ocrelizumab ist ein gentechnisch hergestellter, humanisierter Antikörper. „Humanisiert“ bedeutet in diesem Zusammenhang, dass der ursprünglich von der Maus stammende Antikörper so verändert wurde, dass er größtenteils menschlich ist. Ocrelizumab entfernt bestimmte weiße Blutkörperchen (Leukozyten, speziell B-Lymphozyten) aus dem Blut und Organen. Ocrelizumab ist eine Weiterentwicklung von Rituximab.
Wie wirkt Ocrelizumab?
Ocrelizumab richtet sich gezielt gegen bestimmte Immunzellen, die B-Lymphozyten, die ein Molekül namens CD-20 auf ihrer Außenhülle tragen. Es wird vermutet, dass diese Immunzellen bei MS maßgeblich an der Schädigung der Myelinscheiden und Nervenzellfortsätze sowie der daraus entstehenden Behinderung beteiligt sind. Ein Teil dieser Abwehrzellen wird durch Ocrelizumab zerstört. Dieser Effekt der Verminderung von B-Lymphozyten hält über viele Monate an.
Für wen ist Ocrelizumab zugelassen?
Ocrelizumab ist zum einen für „Patienten mit schubförmiger Multipler Sklerose mit aktiver Erkrankung, definiert durch klinischen Befund oder Bildgebung“ zugelassen.
Des Weiteren besteht die Zulassung „zur Behandlung erwachsener Patienten mit primär progredienter MS, charakterisiert anhand der Krankheitsdauer und dem Grad der Behinderung sowie Bildgebungsmerkmalen, die typisch für Entzündungsaktivität sind.“
Das Krankheitsbezogene Kompetenznetz Multiple Sklerose (KKNMS) hat diese breite Zulassung in seinen Therapieempfehlungen kritisch kommentiert und empfohlen, Ocrelizumab im Wesentlichen nach den Einschlusskriterien der Therapiestudien zu geben. Bei höherem Lebensalter (über 55 Jahre), längerer Krankheitsdauer (mehr als 15 Jahre) oder einem höheren EDSS (höher als 6,5, entsprechend 100m Gehstrecke mit Hilfe) muss eine strenge Nutzen-Risiko Abwägung vorgenommen werden.
Wie wird Ocrelizumab verabreicht?
Ocrelizumab wird als Infusion über eine Vene (intravenös) verabreicht. Die erste Dosis Ocrelizumab (600 mg) wird auf zwei Gaben verteilt. Es werden jeweils 300 mg im Abstand von 14 Tagen verabreicht. Danach erfolgt alle sechs Monate eine Infusion von 600 mg Ocrelizumab .
Direkt vor dem Beginn jeder Ocrelizumab-Infusion wird 100 mg Kortison (Wirkstoff: Methylprednisolon) verabreicht. Das reduziert das Risiko von möglichen Infusionsreaktionen wie Juckreiz oder Ausschlag gegenüber Ocrelizumab. Aus dem gleichen Grund wird meist ein Antiallergikum (bspw. 2mg Clemastin) gegen mögliche Überempfindlichkeitsreaktionen gegeben. Zur Vorbeugung von Fieber und ähnlichen Beschwerden können darüber hinaus 1000mg Paracetamol oder 800mg Ibuprofen verabreicht werden. Alle drei Medikamente erfolgen als Kurzinfusion über die Vene.
Die Verabreichung der Vormedikamente sollte etwa eine Stunde vor Ocrelizumab-Gabe begonnen werden, die anschließende Ocrelizumab-Infusion dauert etwa drei Stunden. Im Anschluss soll eine Nachbeobachtung von einer Stunde erfolgen, so dass insgesamt ca. 5 Stunden Überwachung in der Praxis oder im MS-Zentrum nötig sind.
Hier sehen Sie ein Foto der Medikamentenpackung (links) sowie des Infusionsfläschchens (rechts) von Ocrevus®:
Bildquelle: Pharmaphorum
Wie wirksam ist Ocrelizumab bei primär progredienter MS?
Hinweis: Der Effekt auf die Behinderung war nach der Analysemethode in der Studie (die sogenannte Hazard Ratio) signifikant. Berechnet man den Nutzen durch den Vergleich der Anzahlen von Patienten ohne Zunahme der Behinderung, so ist dieser Effekt statistisch nicht sicher (nicht signifikant). Deshalb wird der Nutzen (grünes Männchen s.o. in der Grafik am Kapitelanfang) hier transparent dargestellt.
1. Wirkung auf die Zunahme der Behinderung
Die Zunahme der Behinderung wurde in der ORATORIO-Studie[6] mit Hilfe der EDSS gemessen, einer Behinderungsskala von 0 bis 10 (wobei 0 keiner Behinderung entspricht). Die folgende Grafik zeigt, wie viele Patienten nach 2 Jahren Therapie mit Ocrelizumab oder Placebo keine Zunahme der Behinderung hatten. Dargestellt ist der absolute Nutzen (absolute Risikoreduktion).
Hier finden Sie auch einige Angaben zum Nutzen von Medikamenten bei anderen Erkrankungen, damit Sie einen Eindruck bekommen, wie groß die Therapieeffekte bei MS im Vergleich zu anderen Therapien sind.
Im Folgenden wird die Entwicklung der Behinderung bezogen auf 100 Patienten beschrieben:
- 6 von 100 Patienten haben durch die Einnahme von Ocrelizumab keine Zunahme der Behinderung
- 33 von 100 Patienten haben trotz der Ocrelizumab-Therapie eine Zunahme der Behinderung
- 61 von 100 Patienten profitieren nicht von der Therapie, sie haben unabhängig von der Therapie keine Zunahme der Behinderung.
Der tatsächliche Therapieeffekt zeigt sich, wenn man die Anzahl der Patienten mit einer Behinderungszunahme in der Ocrelizumab-Gruppe (33) von denen in der Placebo-Gruppe (39) abzieht. Tatsächlich profitieren 39 – 33, also 6 von 100 Patienten von der Therapie. Das entspricht dem absoluten Nutzen (oder auch der absoluten Risikoreduktion).
2. Wirkung auf die MRT
In der MRT treten Kontrastmittelanreicherungen und sogenannte T2-Herde auf, die als Ausdruck der Entzündung bei MS betrachtet werden. Dabei können Herde größer werden oder ganz neu auftreten.
Der Anteil von Patienten ohne neue oder vergrößerte T2-Herde lag unter Ocrelizumab bei 75% und bei 32% unter Placebo.
58% der Patienten aus der Placebo-Gruppe und 93% der Patienten aus der Ocrelizumab-Gruppe hatten keine Kontrastmittel-anreichernden Läsionen. Dieser Unterschied ist nicht signifikant, das heißt, er könnte auch auf Zufall beruhen.
Im Glossar finden Sie Daten zu dem Anteil der Patienten, bei denen es über 2 Jahre keine Anzeichen einer Krankheitsaktivität gab (NEDA - no evidence of disease activity).
Zulassungsstudien
Die Wirkung von Ocrelizumab auf die Zunahme der Behinderung wurde in einer Zulassungsstudie (ORATORIO[6]) für Patienten mit primär progredienter MS geprüft und die Ergebnisse im Jahr 2016 veröffentlicht. Es wurden 732 Patienten mit primär progredienter MS über einen Zeitraum von zwei Jahren untersucht. In die Studie eingeschlossen waren auch viele Patienten, bei denen sich die Behinderung in den letzten Jahren nicht verändert hatte. Dabei wurden die Patienten im Verhältnis 2:1 auf eine Ocrelizumab (600mg)- und eine Placebo-Gruppe verteilt. Doppelt so viel Patienten bekamen also Ocrelizumab wie Placebo. Die Patienten wurden zufällig einer der beiden Behandlungsgruppen zugeteilt, ohne sie darüber zu informieren, ob sie das Medikament oder ein Placebo bekamen.
In der ORATORIO-Studie zeigte sich eine schwach überlegene Wirksamkeit von Ocrelizumab gegenüber Placebo. Im Folgenden stellen wir die Ergebnisse der Studie dar.
Welche Nebenwirkungen hat Ocrelizumab bei primär progredienter MS?
Bei wie vielen Patienten traten Nebenwirkungen auf?
In der ORATORIO-Studie[6] hatten 95% der Patienten, die Ocrelizumab einnahmen, Nebenwirkungen. In der Placebo-Gruppe traten bei 90% der Patienten Nebenwirkungen auf. Dieser Unterschied war jedoch nicht signifikant, das heißt, er kann auch auf Zufall beruhen.
Grundsätzlich ist wichtig zu wissen, dass Nebenwirkungen in Studien nicht nur bei den Patienten auftreten, die ein neues Medikament erhalten, sondern auch in der Studiengruppe mit einem bekannten Medikament oder Placebo.
Bei wie vielen Patienten führten die Nebenwirkungen zum Therapieabbruch?
In der Ocrelizumab-Gruppe brachen 4% der Patienten die Therapie aufgrund von Nebenwirkungen ab, in der Placebo-Gruppe waren es 3%. Auch dieser Unterschied war nicht signifikant.
Häufige Nebenwirkungen
In der Tabelle sind Nebenwirkungen aufgeführt, die aus der Zulassungsstudie ORATORIO berichtet wurden und bei mindestens 2% der Patienten auftraten. Angegeben ist die Patientenzahl von 100 Patienten. In der Grafik zu Anfang des Kapitels sowie in der Faktenbox weiter unten werden jedoch lediglich die wichtigsten Nebenwirkungen dargestellt.
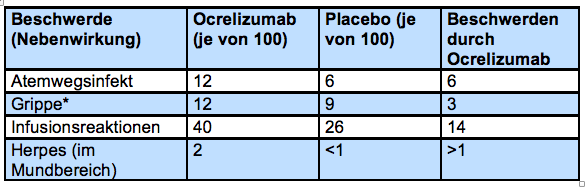
* Bei diesen Nebenwirkungen war der Unterschied zwischen der Ocrelizumab- und der Placebogruppe statistisch nicht signifikant.
Laborwertveränderungen
Bei den Laborwerten sind nur Veränderungen bei den weißen Blutzellen (Lymphozyten) berichtet. Hier ist innerhalb von 2 Wochen nach Therapie eine bestimmte Untergruppe der B-Lymphozyten nicht mehr nachweisbar. Der Effekt hielt während der Therapie bis zum Studienende an.
Infusionsreaktionen
Infusionsreaktionen traten unter Ocrelizumab häufiger auf als unter Placebo. Dies waren z.B. Juckreiz, Ausschlag, Hautreizung, Kopfschmerz, Müdigkeit, Schwindel, Luftnot, Übelkeit, Herzrasen. Es traten keine lebensbedrohlichen oder tödlichen Infusionsreaktionen auf, die Reaktionen waren überwiegend leicht bis moderat.
Am häufigsten zeigten sich Infusionsreaktionen bei der ersten Ocrelizumab-Gabe, bei weiteren Ocrelizumab-Gaben traten Infusionsreaktionen seltener auf und waren weniger schwer.
Infektionen
Atemwegsinfekte traten unter Ocrelizumab häufiger auf, mit einem Unterschied von 6%.
Ebenfalls kam es bei Patienten der Ocrelizumab-Gruppe mit 2% häufiger zu Lippen-Herpes im Bereich des Mundes als bei Patienten der Placebo-Gruppe mit weniger als 1%. Insgesamt traten Herpes-Infektionen bei Einnahme von Ocrelizumab nicht vermehrt auf.
Auch schwere Infektionen traten mit Ocrelizumab nicht häufiger auf als bei Einnahme von Placebo.
Schwere Nebenwirkungen und Todesfälle
Schwere Nebenwirkungen (schwere Infektionen, schwere Infusionsreaktionen, Krebs) kamen unter Ocrelizumab nicht statistisch gehäuft vor. In der Placebo-Gruppe kam es bei 22 von 100 Patienten zu schweren Nebenwirkungen, in der Ocrelizumab-Gruppe bei 20 von 100 Patienten.
Während der Studie traten 5 Todesfälle auf, einer davon in der Placebo-Gruppe, 4 in der Ocrelizumab-Gruppe. Die Ursachen waren in der Placebo-Gruppe: Verkehrsunfall, in der Ocrelizumab-Gruppe 1 Lungenembolie, 2 Lungenentzündungen, 1 Bauchspeicheldrüsenkrebs.
Krebserkrankungen
Während der Studie traten bei 11 Patienten, die Ocrelizumab erhielten, bösartige Tumoren auf und nur bei 2 Patienten mit Placebo.
Bei Ocrelizumab waren dies 4x Brustkrebs, 3x Hautkrebs, 1x Lymphdrüsenkrebs, 1x Gebärmutterkrebs, 1x Sarkom, 1x Bauchspeicheldrüsenkrebs. In der Placebo-Gruppe waren dies 1x Brustkrebs und 1x Gebärmutterhalskrebs. Dieser Unterschied ist jedoch statistisch nicht signifikant. Dennoch ist zu beachten, dass alle Medikamente, die das Immunsystem beeinflussen, das Krebsrisiko erhöhen können. Dies kann aber nur in Langzeitdatensammlungen geklärt werden.
Nach Abschluss aller 3 Ocrelizumab-Studien (siehe dazu auch im Kapitel 7.3. "Therapie der schubförmigen MS - Ocrelizumab") wurden 6 weitere Fälle von Hautkrebs unter Ocrelizumab berichtet.
Welche neuen Nebenwirkungen wurden nach Abschluss der Zulassungsstudien berichtet?
Bei sechs Patienten, die mit anderen Immuntherapien vorbehandelt wurden, wurde eine progressive multifokale Leukenzephalopathie (PML) festgestellt (Stand: September 2018). Diese Patienten hatten teilweise schubförmige aber auch sekundär und primär progrediente MS-Verläufe. Die wissenschaftliche und behördliche Einschätzung ist hier, dass alle Patienten schon vor der Ocrelizumab-Gabe eine PML unter Natalizumab (5 Fälle) oder Fingolimod (1 Fall) entwickelt hatten.
Worauf muss bei der Therapie mit Ocrelizumab geachtet werden?
Unter welchen Umständen sollte Ocrelizumab nicht eingenommen werden?
Ocrelizumab sollte nicht eingenommen werden
- bei schweren Infektionen z.B. Tuberkulose, Hepatitis oder HIV
- bei geschwächtem Immunsystem, oder wenn derzeit oder kürzlich Medikamente, die das Immunsystem schwächen, eingenommen werden bzw. wurden
- wenn innerhalb von 6 Wochen eine Impfung geplant ist oder eine Impfung durchgeführt wurde
- während der Schwangerschaft und Stillzeit
- bei Bestehen einer Krebserkrankung
Worauf ist bei Therapiebeginn zu achten?
Weil Ocrelizumab das Immunsystem hemmt, sollten vor Therapiebeginn alle Standardimpfungen durchgeführt werden, die die STIKO (Ständige Impfkommission) für Menschen empfiehlt, deren Immunsystem teilweise blockiert werden soll.
Falls der Antikörperschutz gegen Windpocken (VZV) im Blut nicht ausreicht, sollte vor Beginn der Therapie eine Impfung erfolgen. Die Therapie mit Ocrelizumab sollte erst nach erfolgreicher Impfung, frühestens nach 6 Wochen begonnen werden.
Bei Patienten, die bereits eine immunmodulierende oder –supprimierende Therapie erhalten haben, müssen in der Regel Sicherheitsabstände zwischen den Therapien eingehalten werden, die sich nach der Wirkdauer der Medikamente richten (siehe unten). Eine Kurzzeitbehandlung mit Kortikosteroiden (Kortison), z.B. zur Schubtherapie, ist auch während der Behandlung möglich.
Welche Sicherheitsabstände müssen eingehalten werden?
Bei Patienten, die bereits eine Therapie erhalten haben, die das Immunsystem beeinflusst oder hemmt, müssen Sicherheitsabstände eingehalten werden. Diese richten sich nach der Wirkdauer der Medikamente. Die Wartezeit nach Empfehlungen des KKNMS beträgt nach der Behandlung mit...
- Dimethylfumarat bis zur Normalisierung des Blutbildes
- Teriflunomid ca. 4 Wochen (nach Auswaschen).
- Fingolimod mindestens 4 Wochen.
- Natalizumab mindestens 6-8 Wochen.
- Azathioprin, Ciclosporin A, Cyclophosphamid, Methotrexat und Mitoxantron mindestens 3 Monate.
- Cladribin mindestens 6 Monate.
- Alemtuzumab mindestens 6-12 Monate.
- Rituximab 6 Monate.
Bei der vorherigen Verwendung von Beta-Interferonen oder Glatirameracetat müssen, solange sich etwaige Blutbildveränderungen normalisiert haben, keine Sicherheitsabstände eingehalten werden.
Was muss während der Therapie kontrolliert werden?
Das KKNMS empfiehlt:
GRAFIK SICHERHEITSUNTERSUCHUNGEN
Ocrelizumab - Häufig gestellte Fragen
Wie lange wird behandelt?
Ocrelizumab wird, genau wie andere immunmodulierende Therapien der MS, als Dauertherapie eingesetzt. Nutzen und Risiko der Einnahme müssen laufend überprüft werden. Ein Abschätzen des Nutzens ist oft frühestens nach einem Jahr möglich. Als Hinweise für eine Wirksamkeit werden bei schubförmiger MS Schubfreiheit und das Fehlen neuer Herde in der MRT angesehen. Deshalb empfiehlt das KKNMS eine Ausgangs-MRT des Kopfes und eine MRT nach 6, 12 und 24 Monaten, um Nutzen und auch mögliche Risiken abzuschätzen
Schwangerschaft und Stillzeit
Ocrelizumab sollte in Schwangerschaft und Stillzeit nicht angewandt werden.
Verlauf von Schwangerschaften in der Zulassungsstudie
In keiner der drei Veröffentlichungen der Zulassungsstudien wurde über Schwangerschaften und deren Verlauf bei Einnahme von Ocrelizumab berichtet. In Sicherheitsanalysen wurde im Herbst 2017 von 25 Schwangerschaften unter Ocrelizumab aus den OPERA-Studien[91] berichtet, die bei Patienten mit schubförmiger MS durchgeführt wurden. Hinweise auf Aborte oder angeborene Fehlbildungen fanden sich nicht.
Impfungen
Patienten, die keinen Schutz gegenüber dem Varicella-Zoster-Virus (VZV) haben, das Windpocken bzw. Gürtelrose auslöst, sollten vor Behandlungsbeginn gegen VZV geimpft werden. Es handelt sich hier um einen Lebendimpfstoff. Ob ein Schutz besteht, kann mit einer Blutuntersuchung (Messung des VZV-Antikörper-Titers) bestimmt werden. Damit die Impfung ihre Wirkung entfalten kann, darf die erste Gabe von Ocrelizumab frühestens sechs Wochen danach erfolgen.
Untersuchungen zu Impfungen und Ocrelizumab zeigen, dass der Impferfolg unter der vollen Wirkung von Ocrelizumab vermindert, aber vermutlich dennoch ausreichend wirksam ist. Insofern sollten alle von der STIKO für Patienten unter einer das Immunsystem unterdrückenden Therapie empfohlenen Impfungen einschließlich Pneumokokken vor Therapiebeginn durchgeführt bzw. aufgefrischt werden. Alle Lebendimpfstoffe sollten unter laufender Ocrelizumab-Therapie vermieden werden, da Patienten möglicherweise keine ausreichende Abwehr haben und durch die eigentlich harmlosen Impferreger krank werden könnten.
Verhalten bei Infektionen
Ocrelizumab sollte nicht bei einem schweren, fieberhaften Infekt gegeben werden.
Welche Alternativen bestehen zu Ocrelizumab?
Bei primär progredienter MS ist Ocrelizumab das einzig zugelassene Medikament. Wie der Verlauf ohne Medikament zumindest kurzfristig aussieht, kann man aus den Daten der Zulassungsstudie nicht abschätzen: Über 2 Jahre blieben in der Placebo-Gruppe 61 von 100 Patienten ohne Zunahme der Behinderung.
Ocrelizumab bei primär progredienter MS - Alles auf einen Blick

